Enolasen
Enolasen (synonym Phosphopyruvat-Hydratase) sind eine Gruppe von Enzymen, welche die Umwandlung von 2-Phosphoglycerat (2-PG) zu Phosphoenolpyruvat (PEP), dem neunten und vorletzten Schritt der Glykolyse, katalysieren.
| Enolasen | ||
|---|---|---|
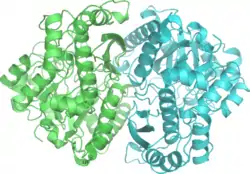 | ||
| Bändermodell der Enolase von Saccharomyces cerevisiae, nach PDB 2ONE | ||
| Enzymklassifikation | ||
| EC, Kategorie | 4.2.1.11, Lyase | |
| Substrat | D-2-Phosphoglycerat | |
| Produkte | Phosphoenolpyruvat + H2O | |
| Vorkommen | ||
| Übergeordnetes Taxon | Lebewesen | |
Eigenschaften
Die chemische Reaktion, die von der Enolase katalysiert wird, ist:
- D-2-Phosphoglycerat ⇌ Phosphoenolpyruvat + H2O
Enolase gehört zur Familie der Lyasen, genauer gesagt zu den Hydrolyasen, die Kohlenstoff-Sauerstoff-Bindungen spalten. Der systematische Name dieses Enzyms ist 2-Phospho-D-Glycerat-Hydro-Lyase (phosphoenolpyruvatbildend).
Die Reaktion ist reversibel, abhängig von den Konzentrationen der Substrate in der Umgebung.[1] Der optimale pH-Wert für das menschliche Enzym liegt bei 6,5.[2] Enolase ist in allen Geweben und Organismen vorhanden, die zur Glykolyse oder Fermentation fähig sind. Das Enzym wurde 1934 von Lohmann und Meyerhof entdeckt[3] und wurde seitdem aus einer Vielzahl von Quellen isoliert, einschließlich menschlicher Muskeln und Erythrozyten.[2] Beim Menschen ist ein Mangel an ENO1 mit der hereditären hämolytischen Anämie verbunden, während ein ENO3-Mangel mit der Glykogenspeicherkrankheit Typ X verbunden ist.
Struktur
Beim Menschen gibt es drei Untereinheiten der Enolase, α, β und γ, die jeweils von einem separaten Gen kodiert werden und sich zu fünf verschiedenen dimeren Isoenzymen verbinden können: αα, αβ, αγ, ββ und γγ.[1][4] Drei dieser Isoenzyme (alle Homodimere) sind in erwachsenen menschlichen Zellen häufiger zu finden als die anderen:
- αα oder nicht-neuronale Enolase (NNE). Auch bekannt als Enolase 1. Wird in einer Vielzahl von Geweben gefunden, einschließlich Leber, Gehirn, Niere, Milz und Fettgewebe. Sie ist in gewissem Umfang in allen normalen menschlichen Zellen vorhanden.
- ββ oder muskelspezifische Enolase (MSE). Auch bekannt als Enolase 3. Dieses Enzym ist weitgehend auf den Muskel beschränkt, wo es in sehr hohen Konzentrationen vorhanden ist.
- γγ oder neuronenspezifische Enolase (NSE). Auch bekannt als Enolase 2. Wird in sehr hohen Konzentrationen in Neuronen und neuralem Gewebe exprimiert, wo es bis zu 3 % des gesamten löslichen Proteins ausmachen kann. In den meisten Säugetierzellen wird sie in viel geringerem Maße exprimiert.
Einzelnachweise
- V. Pancholi: Multifunctional alpha-enolase: its role in diseases. In: Cellular and molecular life sciences : CMLS. Band 58, Nummer 7, Juni 2001, S. 902–920, doi:10.1007/pl00000910, PMID 11497239.
- R.K.J. Hoorn, J.P. Flikweert, G.E.J. Staal: Purification and properties of enolase of human erythrocytes. In: International Journal of Biochemistry. 5, 1974, S. 845, doi:10.1016/0020-711X(74)90119-0.
- K. Lohman, O. Meyerhof: Über die enzymatische Umwandlung von Phosphoglyzerinsäure in Brenztraubensäure und Phosphorsäure. (1934) In: Biochem. Z. 273, S. 60–72.
- M. Peshavaria, I. N. Day: Molecular structure of the human muscle-specific enolase gene (ENO3). In: The Biochemical journal. Band 275 ( Pt 2), April 1991, S. 427–433, doi:10.1042/bj2750427, PMID 1840492, PMC 1150071 (freier Volltext).