Elektrochemische Scan-Mikroskopie
Elektrochemische Scan-Mikroskopie (SECM) (englisch: scanning electrochemical microscopy) ist eine Technik aus der größeren Klasse der Rastersondenmikroskopie, die man anwendet, um das Verhalten von Phasengrenzen flüssig/fest, flüssig/gasförmig und fest/fest zu untersuchen.[1][2][3][4][5] Die Anfänge dieser Methode gehen auf Allen J. Bard, einen Elektrochemiker der Universität Texas zurück.[6] Seitdem die Technik auch theoretisch untermauert wurde, fand sie breite Anwendung in Chemie, Biologie und Materialwissenschaften. Hochaufgelöste elektrochemische Signale können aufgezeichnet werden, indem man mit einer Ultramikroelektrode (UME) den Strom als eine Funktion der Position mit der Elektrodenspitze an der betreffenden Stelle des Substrates misst. Die Interpretation des SECM-Signals basiert auf dem Konzept des diffusionsbegrenzten elektrischen Stroms.[7] Zweidimensionale Rasterscan-Informationen können verwendet werden, um Bilder der Oberflächenreaktivität und der chemischen Kinetik zu messen. Eine ergänzende Methode zur Oberflächencharakterisierung ist die Oberflächenplasmonenresonanzspektroskopie,[8] Elektrochemische Rastertunnelmikroskopie (ESTM)[9], die Rasterkraftmikroskopie, auch atomare Kraftmikroskopie oder Atomkraftmikroskopie (engl.atomic/scanning force microscopy, Abkürzung (AFM)),[10] bei der Untersuchung von verschiedenen Oberflächenphänomenen. Zusätzlich zum Gewinn an Information über die Oberflächenstruktur wird SECM oft verwendet, um die Oberflächenreaktivität von Feststoffen, elektrochemisch wirksamen Katalysatoren, Enzymen und anderen biophysikalischen Systemen zu testen.[11] SECM und Variationen der Technik wurden verwendet bei Mikrofabrikation, Oberflächenveredelung und Mikrostrukturierung.[12]
Geschichte
Die Notwendigkeit von Ultramikroelektroden (UME) um 1980 ging einher mit der Entwicklung hochsensibler elektroanalytischer Technik wie SECM. Die Anwendung von Spitzen machte die Untersuchung von schnellen elektrochemischen Reaktionen möglich. Das erste SECM-Experiment wurde 1986 von Engstrom durchgeführt, der eine direkte Beobachtung von Reaktionsprofilen und kurzlebigen Zwischenstufen erzielte.[13] Gleichzeitige Experimente von Alan J. Bard mit dem elektrochemischen Rastertunnelmikroskop (ESTM) zeigten einen Strom über große Entfernungen "Elektrodenspitze zu Probe", der nicht mit dem Tunneleffekt erklärbar war. Dieses Phänomen beruhte auf dem Faraday-Strom, der eine sorgfältige Analyse bei der elektrochemischen Mikroskopie ermöglichte.[14] Die theoretische Basis wurde 1989 von Bard gelegt, als erstmals den Begriff elektrochemische Scan-Mikroskopie prägte. Zusätzlich zum seinerzeit gebräuchlichen Datensammelmodus, erweiterte Bard die weitverbreitete Verwendung des SECM durch Ergänzung verschiedener Einstellungen.[6] Als die theoretische Hintergrund erläutert war, wuchs die Zahl der jährlichen Publikationen von 10 auf 80 im Jahr 1999, als das erste SECM käuflich erwerblich war.[15] Die Beliebtheit des SECM wächst aufgrund des Fortschritts in Theorie und Technologie, die die experimentellen Möglichkeiten erweitern auf eine vielfältigere Substanzauswahl und auf eine feinere Genauigkeit.[16]
Anwendungsprinzip
Das elektrische Potential wird durch die UME-Spitze in einer gesättigten Lösung erzeugt, die z. B. das Redoxpaar (Fe2+/Fe3+) enthält. Wenn die angelegte Spannung negativ genug ist, wird (Fe3+) an der Elektrodenspitze zu (Fe2+) reduziert und erzeugt dabei einen diffusions-kontrollierten Strom.[13] Der gemessene Strom basiert auf dem Ionenstrom in der Lösung zur Elektrode und wird mathematisch beschrieben durch die Gleichung:
wobei iT,∞ der diffusionskontrollierte Strom ist und, n die Anzahl der Elektronen, die zur Elektrodenspitze gelangt (O + ne− → R), F ist die Faraday-Konstante, C ist die Konzentration der oxidierten Spezies in Lösung, D ist der Diffusionskoeffizient und a ist der Radius der UME-Elektrodenspitze. Um die entsprechende Oberfläche zu untersuchen, wird die Spitze auf die Oberfläche zu bewegt und erzeugt so den Strom.
Die zwei Operationsmodi sind der Feedback-Modus und der Sammel-Modus.
Feedback Modus
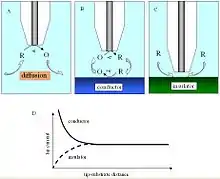
In einer gesättigten Lösung wird die oxidierte Spezies an der Elektrodenspitze reduziert, wobei sie einen Strom erzeugt, der durch die Halbzellendiffusion limitiert ist. Wenn sich die Elektrodenspitze einer leitfähigen Substanz in der Lösung nähert, wird die an der Spitze gebildete reduzierte Spezies an der leitfähigen Oberfläche oxidiert, indem sie an der Spitze einen Strom erzeugt und damit eine positive Feedback-Schleife erzeugt.[6] Der gegenteilige Effekt wird beobachtet, wenn man isolierende Oberflächen untersucht, da die oxidierte Spezies nicht regeneriert werden kann und die Diffusion zur Elektrode verhindert wird (als Ergebnis einer physikalischen Hemmung), während die Spitze sich dem Substrat nähert und dabei eine negative Feedback-Schleife erzeugt und den Strom an der Spitze verringert. Ein zusätzlich zu beachtender Parameter, wenn man isolierende Oberflächen untersucht, ist der Parameter rg, da er zur physikalischen Hemmung der Diffusion beträgt.
Die Änderung des Stroms an der Elektrodenspitze kann als Funktion der Entfernung d als Näherungskurve aufgezeichnet werden. Aufgrund der Konzentrationsabhängigkeit der SECM-Messungen kann man auch Elektron-Transfer Kinetik untersuchen.[17]
Sammel-Modus
Ein anderer Arbeitsmodus wird angewendet bei der Spitzenerzeugung/Substratsammlung (TG/SC). In diesem Modus wird die Spitze mit einer für die Elektrodenreaktion genügend großen Spannung gehalten, so dass ein Produkt erzeugt werden kann, das mit dem Substrat reagieren kann oder so, dass das Elektrodenprodukt vom Substrat aufgesammelt werden kann.[6] Die umgekehrte Methode ist die Substraterzeugung/Spitzensammlung (SG/TC), wobei das Substrat die Spezies erzeugt, die an der Spitze gemessen (bzw. gesammelt) wird.[7]
Zwei Ströme werden erzeugt: der Spitzenstrom iT, und der Substratstrom iS. Sobald das Substrat viel großer ist als die Spitze, ist die Effektivität des Sammelns iS/iT gleich 1, wenn keine Reaktion abläuft während des Übergangs der spitzenerzeugten Spezies zum Substrat. Wenn die Entfernung Spitze-Substrat d abnimmt, nähert sich die Sammeleffektivität 1 an.
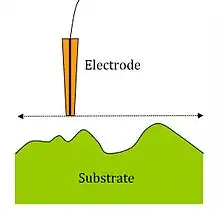
SECM Bildgebung
Änderung des Stroms als Funktion des Abstandes zwischen Elektrodenspitze und Lösungsoberfläche erlaubt die Abbildung von isolierenden und leitenden Oberflächen. Man erhält Informationen über Beschaffenheit und Reaktivität, indem man die Spitze über die Oberfläche bewegt und so den Strom erzeugt. Die gebräuchlichste Scanmethode ist die bei konstanter Höhe,[7] wobei die Spitzenhöhe unverändert ist, während die Oberfläche in der X-Y-Ebene gescannt wird.[7] Eine Alternative ist die Messung bei konstantem Strom, wobei man versucht, einen konstanten Strom während der Veränderung der Entfernung Substrat/Spitze zu erzeugen und die Änderungen von d aufzuzeichnen.
Die Auflösung ist abhängig vom Spitzenradius, der Entfernung des Substrates zur Spitze, der Präzision der elektronischen Instrumente und anderen Dingen.
Instrumenteller Aufbau
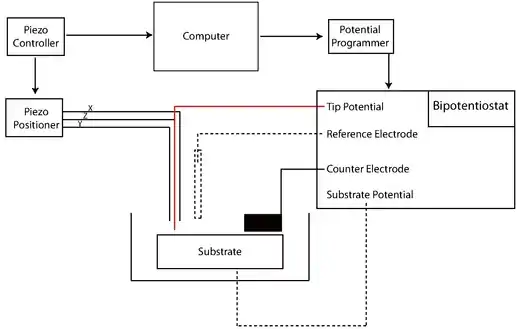
Die frühen SECMs wurden von einzelnen Arbeitsgruppen mit den allgemeingebräuchlichen Geräten konstruiert: Potentiostat und Bipotentiostat, Spannungsgeber, Stromverstärker, piezoelektrischen Positionierer und piezoelektisches Messgerät, Computer und die UME (Elektrode).[4] Manche SEMC-Experimente sind hoch spezifisch und Eigenbau von SEMCs bleibt gebräuchlich. Die Entwicklung neuer Techniken in Richtung Nanofabrikation der Elektroden war lange im Brennpunkt der einschlägigen Literatur wegen der entscheidenden Vorteile inklusive der hohen Konzentrationen und der niedrigschwelligen Absorptionen an Reaktanten bei kinetischen Experimenten.[18][19] Zusätzlich zu der für die hohe Auflösung erforderlichen geringen Spitzengröße tendiert die SECM-Forschung zu kleineren und schnelleren Phänomenen. Die folgenden Methoden geben einen kurzen Überblick über die Herstellungstechniken auf sich rasant entwickelnden Feld.
Vorbereitung der Elektroden
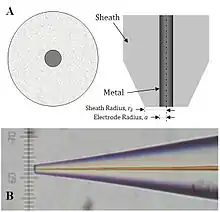
Die typische Herstellung einer mikroskaligen Elektrode erfolgt durch Erhitzen eines Mikro-Karbonfaserkabels in einer Glaskapillare unter Vakuum. Diese Spitze kann verknüpft werden mit einer etwas größeren Kupferelektrode mit Hilfe von Silberepoxid und wird dann poliert, so dass man eine scharfe Spitze erhält. Nanofabrikation der Elektroden erfolgt, indem man das Metall mit NaCN/NaOH anätzt. Das angeätzte Metallkabel wird dann mit Wachs überzogen, poliert und mit Paraffin, Glas oder Polymethylstyrol oder Polyimid ummantelt,[20] mit Phenol elektropolymerisiert und elektrophoretisch gefärbt/lackiert.[21] Nanospitzen, die auf diese Art produziert werden, sind konisch. Scheibenförmige Spitzen erhält man, indem man glasummantelte Elektroden wie eine Mikropipette zieht. Nanoskalige Elektroden erlauben hochaufgelöste Experimente für biologische Anwendungen im Mikromaßstab oder Einzelmolekülexperimente. Auch Experimente, bei denen die Spitze in eine Mikrostruktur eintaucht (z. B. Polymerfilme mit einem fixierten Redoxzentrum), um kinetische Parameter und Konzentrationen zu prüfen, erfordern ebenso nanoskalige Elektroden.[22] Jedoch bleiben Mikroelektroden ideal für quantitative Kinetik-Experimente wegen der größeren Oberfläche.
Unterschiedliche Arten von Elektroden wurden entwickelt zusätzlich zu den unterschiedlichen Größenvarianten. SECM-AFM-Untersuchungen können als Sensor oder als Elektrode verwendet werden, bedingt durch das geschliffene, angeätzte Metallkabel mit der Ummantelung und dem elektrophoretisch hergestellten Lack. In diesem System wird das glatte Kabel als flexibles Cantilever verwendet, um die Gegenkraft der Probe (AFM) zu messen, während das Elektrodenkabel den Strom misst.[2] Darüber hinaus kann die SECM-Funktionalität in ein Standard-AFM integriert werden, indem man die Oberfläche mit einem leitfähigen Material veredelt oder eine isolierte Spitze mit einem fokussierenden Ionenstrahl behandelt. Erst kürzlich wurde mit Elektronenstromlithographie gezeigt, dass man reproduzierbare SECM-AFM-Untersuchungen mit Siliziumdioxid-Wafern durchführen kann.[23]
Bilder von der chemischen Umgebung unabhängig von lokalen Topographien ist wünschenswert, um größere oder unebene Oberflächen zu untersuchen. Softstyleuntersuchungen wurden kürzlich entwickelt, indem man eine mikrofabrizierte Spur auf einem Polyethylenterephthalat-Blatt mit leitfähiger Kohlemine erzeugte. Laminierung mit einem Polymerfilm erzeugte einen v-formigen Stift, der abgeschnitten war, um die Kohlespitze freizulegen. Das flexible Design erlaubt einen konstanten Kontakt von Spitze und dem zu untersuchenden Substrat. Wenn die Apparatur mit der Spitze über die Probe fährt, zeigen sich die topographischen Unterschiede bei einem nahezu konstanten Spitze-Substrat-Abstand, d.[24]
Mikro-ITIES-Untersuchungen sind eine andere spezielle Untersuchungsmethode, die die Phasengrenze zwischen zwei unmischbaren Elektrolytlösungen ausnutzt. Die Spitze bildet eine ausgezogene Pipette, die eine metallische Zählelektrode enthält, und wird verwendet, um Elektron- und Ionentransfer-Prozesse während des Mischvorgangs zu messen, während eine Zähl-Referenzelektrode in die unmischbare Flüssigkeit taucht.[1]
Oft wird eine Phasengrenze flüssig/flüssig und gasförmig/flüssig mit einer SECM-Unterwasserelektrode gemessen.[25] Die wachsende Komplexität der Elektroden sinkt mit der Größe und braucht hochauflösende Technik. Rasterkraftmikroskopie (scanning electron microscopy, SEM), Cyclovoltammetrie und SECM-Näherungskurven werden angewendet, um die Dimensionen und Geometrien der durchgeführten Versuche zu beschreiben.
Potentiostat
Der Potentiostat misst die Spannung des drei-Elektrodensystems für voltammetrische Experimente. Die UME ist die Arbeitselektrode, um eine kontrollierte Spannung am Substrat anzulegen. Die Hilfselektrode (oder Zählelektrode) reguliert den Strom, der an der Arbeitselektrode entsteht, oft durch eine Redoxredaktion mit dem Lösungsmittel oder einem Elektrolytzusatz. Die Spannung wird relativ zu einem genau definierten Reduktionspotential der Referenzelektrode gemessen, durch die selbst kein Strom fließt.
Stellungsregler und Umsetzer
Die SECM verwendet dieselben positionierenden Komponenten, die andere Charakterisierungstechniken verwenden. Präzises Positionieren zwischen Spitze und Probe ist ein entscheidende Faktor, der umgekehrt proportional ist zur Spitzengröße. Die Positionierung der Probe relativ zu einem bestimmten Punkt auf der Materialoberfläche in x-, y- und z-Richtung ist typischerweise eingestellt durch einen Motor für die grobe Positionierung, verknüpft mit einem piezoelektrischen Motor für die Feineinstellung. Genauer gesagt haben die Systeme einen Motor im Zoll-Bereich und einen zusätzlichen Piezo-Motor in z-Richtung. Schrittmotoren mit XYZ-Piezoblock oder geschlossenem Regelkreis sind ebenfalls in Gebrauch.[15]
Anwendungen
SEMC wurde angewendet, um die Oberflächeneigenschaften und die Oberflächenreaktivität eines Feststoffes zu messen, die Kinetik der Dissoziation von Ionenkristallen in wässriger Lösung zu erforschen, elektrokatalytische Prozesse sichtbarzumachen, enzymatische Reaktionen zu veranschaulichen und die Dynamik des Transports über eine Membran oder durch andere biophysikalische Systeme zu untersuchen. Frühe Experimente konzentrierten sich auf die fest/flüssig-Phasengrenze und die Charakterisierung lösungsmittelbasierter elektrochemischer Systeme bei höherer Auflösung und Empfindlichkeit als herkömmliche elektrochemische Systeme typischerweise bieten. Kürzlich wurde eine SEMC-Technik entwickelt, um die chemische Dynamik an Phasengrenzen flüssig/flüssig und flüssig/gasförmig zu untersuchen.
Mikrostruktur
SEMC und Varianten der Technik haben Anwendung gefunden in Mikrofabrikation, Oberflächenveredelung und Mikrostrukturierung.[12] Eine Vielfalt an Oberflächenreaktionen wurde in diesem Zusammenhang erforscht – inklusive Metallzerfall –, außerdem das Ätzen und das Strukturieren von Oberflächen mit Enzymen. Auch die Scanning Probe Lithography (SPL) von Oberflächen kann mit SECM-Technik durchgeführt werden. Wegen der begrenzten Möglichkeiten bei der Mikrofabrikation der UMEs ist die Auflösung vermindert und erfordert größere Größen im Vergleich zu SPL-Techniken. Ein früheres Beispiel zeigte das Muster von Dodecylthiolat, eine selbstorganisierende Monoschicht (SAM), indem man die UME auf einem zweidimensionalen Feld in der Nähe der Oberfläche bewegt und dabei eine Spannung in der Größenordnung des Oxidations- oder Reduktionspotentials anlegt, so dass die chemische Spezies lokal desorbiert wird.[12] Muster im Mikromaßstab werden effektiv auf die Probe (SAM) aufgebracht. Ein besonderer Vorteil der SECM gegenüber früheren SPL-Techniken für die Oberflächenstrukturierung ist, dass man gleichzeitig elektrochemische Informationen erhält, während man lithographisch arbeitet. Andere Studien haben den Nutzen vom SECM bei der Aufbringung von lokalen Goldschichten als Template an Biomoleküle und Fluoreszenzfarbstoffe gezeigt.[26] Solche Techniken wurden vorgeschlagen als potentielle Technik für die Herstellung nanoskaliger Assemblies, da sie es möglich machen, die untersuchten Systeme mit kleinen Goldplättchen zu versehen.
Variationen der SECM wurden verwendet, da man mit der mikropipettenförmigen Spitze räumlich aufgelöste Mikrokristalle auf ein Glas auftragen kann.[27] Hier werden Glaskapillaren im Submikrometermaßstab verwendet, ersetzten die Standard-UME, und erzeugen Femtoliter-große Tropfen, die aus einer Kapillare auf eine leitfähige Oberfläche getropft werden, die als Arbeitselektrode verwendet wird. Bei Kontakt mit einer positiv geladenen Oberfläche, erreichen die kleinen Tropfen der Salzlösung Übersättigung und kristallisieren mit wohldefinierter mikroskaliger Geometrie.
Ionendissoziation
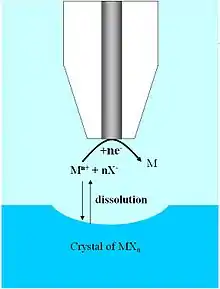
Die Dissoziation von Ionenkristallen in wässriger Lösung ist wichtig für die Charakterisierung des Wirts bei natürlich vorkommenden und synthetischen Wirt-Gast-Systemen.[28] Die hohe räumliche Auflösung und die dreidimensionale Beweglichkeit, die bei der UME gegeben ist, erlaubt es, die Dissoziationskinetik von speziellen Ionenkristallen zu messen, wobei mit frühere Charakterisierungstechniken nur eine Messung der Gesamtmasse möglich war, über die dann gemittelt wurde. Wegen der hohen Massentransfer-Raten, die mit UME und SECM gemessen wurden, ist es möglich, sehr schnelle Reaktionskinetik zu messen. Zusätzlich erlaubt die UME die Messung über einen großen dynamischen Raum und macht damit die Untersuchung von ionischen Feststoffen mit sehr großen Löslichkeitsunterschieden möglich. Die ersten Beispiele für die Anwendung der SECM wurden mit gesättigter Kupfersulfatlösung durchgeführt.[29] Durch Positionierung einer UME und SECM-Konfiguration, ungefähr in der Entfernung des Elektrodenradius von der Kristallfläche des Kupfersulfats, war es möglich, das Dissoziationsgleichgewicht durch lokale Reduktion an der Elektrodenoberfläche zu zerstören. Die Kristallfläche, die in Kupfer- und Sulfationen aufgetrennt ist, zeigt eine sichtbaren Rille und ein chronoampèrmetrisches Signal konnte aufgezeichnet werden als Funktion des Abstandes zwischen Kristall und Elektrode. Nimmt man Reaktionen erster und zweiter Ordnung an, so ergibt sich die Reaktionskonstante aus den gemessenen Daten. Ähnliche Studien wurden an Kristallsystemen ohne unterstützenden Elektrolyten durchgeführt.[30]
Elektrokatalytische Untersuchung
Die Suche nach neuen katalytischen Materialien, welche die für Brennstoffzellen gebrauchten kostbaren Metalle ersetzen, erfordern genaue Kenntnis der Redoxreaktionen auf Metalloberflächen. Noch wichtiger ist die Notwendigkeit, eine Vielzahl neuer elektrokatalytisch wirksamer Substanzen zu untersuchen. Manche Gruppen, die sich mit Elektrokatalyse beschäftigen, haben gezeigt, dass SECM eine schnelle Screening-Technik ist, die lokal quantitative elektrochemische Information über Katalysator-Materialien und Eigenschaften liefert.[31][32]
Eine Vielzahl an Konzepten wurde für eine optimale Auswahl neuer metallischer Elektrokatalysatoren vorgeschlagen. Ein funktionaler, Nicht-SECM-Versuch machte es möglich, dass eine große Anzahl optisch aktiver Katalysatoren untersucht wird, mit einer Technik, die die Protonenproduktion mit protonensensitiven Farbstoffen nachweist.[33] Obwohl diese Technik nützlich ist, fehlt es an exakter quantitativer elektrochemischer Information, die man nur außerhalb des experimentellen Aufbaus erhält. Bard et al. haben nun ein Verfahren entwickelt, das elektrokatalytische Aktivitäten bei großem Volumen mit der SECM messen kann.[31] Mit Näherungsverfahren lassen sich direkte quantitative elektrochemische Informationen von Multikomponentensystemen auf einer schnellen Screening-Plattfrom erzielen. Diese Screening-Verfahren mit hohem Durchsatz ermöglichen eine zuverlässige, effektive und kostenschonende Auswahl an elektrokatalytischen Materialien als Ersatz für Platin und andere kostbare Metalle.
Biologische Analyse
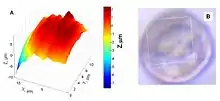
Die Möglichkeit, nichtleitende Oberflächen zu untersuchen, macht SECM zu einer brauchbaren Methode, um Membranen, redoxaktive Enzyme und andere biophysikalische Systeme zu analysieren. Änderungen der intrazellularen Redoxaktivität stehen in Relation mit oxidativem Stress und Krebs. Redoxprozesse in lebenden Zellen können mit SECM untersucht werden, eine nicht-invasive Methode, um intrazellulären Ladungstransfer aufzuzeichnen. Bei solchen Messungen wird die betreffende Zelle auf einer Oberfläche fixiert, mit einer Lösung der oxidierten Form des Redoxpaares benetzt, und der Feedback-Modus wird eingestellt. Eine Spannung wird an die Spitze angelegt, die die oxidierte Spezies reduziert, während der Strom iT erzeugt wird. Wenn das Spitzenprodukt in die Zelle gelangt, wird es dort re-oxidiert durch Prozesse in der Zelle und wieder ausgeschieden. Abhängig von der Konzentrationsrate, mit der das Spitzenprodukt in der Zelle regeneriert wird, ändert sich der Spitzenstrom.[34] Liu et al. wandten diese Methode an und zeigten, dass die Redoxzustände von menschlichen Brustzellen unterschiedliche Konsistenz besitzen (beweglich, unbeweglich und metastatisch). SECM kann nicht nur immobilisierte Zellen, sondern auch die Kinetik immobilisierter redoxaktiver Enzyme untersuchen.[35]
Der Transport von Ionen wie K+und Na+ durch Membranen und andere biologische Phasengrenzen ist für viele Zellen lebenswichtig; SECM wurde angewendet, um den Transport redoxaktiver Spezies durch Zellmembranen zu untersuchen. Im Feedback-Modus wird der Transport von Molekülen durch eine Membran durch das Sammeln der transferierten Spezies an der Elektrodenspitze und durch Bildung eines Konzentrationsgradienten, der Diffusionsprozesse ermöglicht.[4] Die Stromänderungen können als Funktion der Transportrate von Molekülen gemessen werden.
Elektrokatalyse
Die Phasengrenze zwischen zwei nicht mischbaren Elektrolytlösungen kann mit Hilfe von SECM mit Mikro-ITIES untersucht werden. Die Untersuchung findet in einer Phase statt und wird an die Phasengrenze bewegt, während man ein Potential anlegt. Oxidation und Reduktion verändern die Konzentrationen an Substrat, was eine Diffusion von einer Phase in die andere zur Folge hat. Bei naher Spitzen-Phasengrenze-Entfernung können ein Substrat oder Ionen bezüglich ihrer Diffusionsrate zwischen wässriger und organischer Phase untersucht werden.[36] Elektronentransfer wurde ebenfalls mit ITIES erforscht. In diesen Experimenten werden Redoxpaare in zwei verschiedenen Phasen gelöst und der erzeugte Strom mit der ITIES aufgezeichnet.[1] Genau das ist das fundamentale Prinzip bei der Untersuchung von Transportphänomenen in Membranen.
Phasengrenze flüssig/gasförmig
Der soweit größte Gewinn auf diesem Gebiet war die quantitative Analyse von molekularer Bewegung entlang eines einschichtigen Films, um Erkenntnisse über chemische Transporteigenschaften in Zellmembranen und der chemischen Diffusion in die sie umgebende Lösung zu gewinnen.[37]
Obwohl viel Arbeit getan ist auf dem Gebiet der Evaporisation (Verdampfung) durch einfache Membranen, bot die Erfindung der SEMC-Wissenschaftlern die Möglichkeit, die Permeabilität von einfachen Membranen für kleine lösliche Moleküle durch die Phasengrenze zu erforschen. Durch genaues Positionieren einer Unterwasserelektrode neben einer organischen Einfachmembran, die eine Luft-Wasser-Phasengrenze trennt, konnten Wissenschaftler das Diffusionsgleichgewicht von Sauerstoff durch lokale Reduzierung der Sauerstoffmenge in der wässrigen Phase untersuchen, wobei die Diffusion durch die Membran aufgezeichnet wurde.[38] Diffusionsdynamik eines Systems kann veranschaulicht werden durch die Messung eines elektrischen Stroms als Antwort auf die UME mit hoher räumlicher und zeitlicher Auflösung. SECM ist eine ganz passable Möglichkeit für kinetische Studien, da der Strom aufgrund des schnellen Massentransfers mit hoher Sensibilität (in Abhängigkeit von SECM und UME) aufgenommen werden kann. Die Beweglichkeit der UME in alle drei Raumrichtungen bietet eine Untersuchungsmethode, mit der man die Punkte für die Durchlässigkeit messen kann. Eine ähnliche Vorgehensweise wird angewendet für Studien der Phasengrenze flüssig/flüssig und fest/flüssig.
Einzelnachweise
- Unwin, Patrick, Barker, Gonsalves, Macpherson, Slevin: Scanning electrochemical microscopy: beyond the solid/liquid interface. In: Elsevier: Analytica chimica acta. 385, 1999, S. 223–240.
- Zhang,Jie,Barker, Unwin: Measurement of the forward and back rate constants for electron transfer at the interface between two immiscible electrolyte solutions using scanning electrochemical microscopy (SECM): Theory and experiment. In: Electrochemistry Communications. 3, 2001, S. 372–378. doi:10.1016/s1388-2481(01)00173-4.
- Mirkin,Michael,Sun: Kinetics of electron transfer reactions at nanoelectrodes. In: Analytical Chemistry. 78, 2006, S. 6526–6534. doi:10.1021/ac060924q.
- Mirkin, Michael, Peng Sun, Francois O. Laforge: Scanning electrochemical microscopy in the 21st century. In: Physical Chemistry Chemical Physics. 9, 2007, S. 802–823. bibcode:2007PCCP....9..802S. doi:10.1039/b612259k.
- Wittstock, Gunther: Imaging Localized Reactivities of Surfaces by Scanning Electrochemical Microscopy. In: Topics in Applied Physics. 85, 2003, S. 335–366. doi:10.1007/3-540-44817-9_11.
- Bard, Allen, Fan, Fu Ren F., Kwak, Juhyoun., Lev, Ovadia.: Scanning electrochemical microscopy. Introduction and principles. In: Analytical Chemistry. 61, Nr. 2, 1989, ISSN 0003-2700, S. 132–138. doi:10.1021/ac00177a011.
- Bard, Allen: Scanning Electrochemical Microscopy. Marcel Dekker, New York 2001, ISBN 0-8247-0471-1.
- Szunerits, Sabine, Knorr, Nikolaus, Calemczuk, Roberto, Livache, Thierry: New Approach to Writing and Simultaneous Reading of Micropatterns: Combining Surface Plasmon Resonance Imaging with Scanning Electrochemical Microscopy (SECM). In: Langmuir. 20, Nr. 21, 2004, ISSN 0743-7463, S. 9236–9241. doi:10.1021/la0492557.
- Wittstock,Gunther, Thomas H. Treutler: Combination of an electrochemical tunneling microscope (ECSTM) and a scanning electrochemical microscope (SECM): application for tip-induced modification of self-assembled monolayers. In: Electrochimica Acta. 48, 2003, S. 2923 -2932. doi:10.1016/s0013-4686(03)00357-8.
- Mizaikoff, Bertagnolli, Lugstein, Kueng, Kranz: Mapping of enzyme activity by detection of enzymatic products during AFM imaging with integrated SECM–AFM probes. In: Ultramicroscopy. 100, 2004, S. 127–134. doi:10.1016/j.ultramic.2003.10.004.
- Wittstock, Gunther, Burchardt, Malte, Pust, Sascha, Shen, Yan, Zhao, Chuan: Scanning Electrochemical Microscopy for Direct Imaging of Reaction Rates. In: Angewandte Chemie International Edition. 46, Nr. 10, 2007, ISSN 1433-7851, S. 1584–1617. doi:10.1002/anie.2006027500.
- Gorman, Christopher, Stephan, Kramer, Ryan R., Fuierer: Scanning Probe Lithography Using Self-Assembled Monolayers. In: Chemical Reviews. 103, 2003, S. 4367–4418. doi:10.1021/cr020704m.
- Engstrom, R.C., M. Weber, D. J. Wunder, R. Burgess, S. Winguist: Measurements within the diffusion layer using a microelectrode probe. In: Anal. Chem.. 58, Nr. 4, April 1986, S. 844–848. doi:10.1021/ac00295a044.
- Bard, Allen, Hsue-Yang Liu, Fu-Ren F. Fan, Charles W. Lin: Scanning Electrochemical and Tunneling Ultramicroelectrode Microscope for High-Resolution Examination of Electrode Surfaces in Solution. In: J. Am. Chem. Soc.. 108, 1986, S. 3838–3839. doi:10.1021/ja00273a054.
- Mirkin, Michael, Peng Sun, Francois Laforge: Scanning electrochemical microscopy in the 21st century. In: Physical Chemistry Chemical Physics. 9, 30. November 2006, S. 802–23. bibcode:2007PCCP....9..802S. doi:10.1039/b612259k. Abgerufen am 5. Oktober 2011.
- Michael V. Mirkin, Wojciech Nogala, Jeyavel Velmurugan, Yixian Wang: Scanning electrochemical microscopy in the 21st century. Update 1: five years after. In: Physical Chemistry Chemical Physics. Band 13, Nr. 48, 29. November 2011, S. 21196–21212, doi:10.1039/C1CP22376C.
- Bard, Allen J., David O. Wipf: Effect of Heterogeneous Electron-Transfer Rate at the Substrate on the Tip Feedback Current. In: J. Electrochem. Soc.. 138, Nr. 2, 1991, S. 469–474.
- Schuhmann, Wolfgang, Bernardo Ballesteros Katemann, Albert Schulte: Constant-Distance Mode Scanning Electrochemical Microscopy. Part II: High-Resolution SECM Imaging Employing Pt Nanoelectrodes as Miniaturized Scanning Probes. In: Electroanalysis. 16, Nr. 1-2, 2004, S. 60–65. doi:10.1002/elan.200302918.
- Unwin, Patrick, Martin A Edwards, Sophie Martin, Anna L Whitworth, Julie V Macpherson: Scanning electrochemical microscopy: principles and applications to biophysical systems. In: Physiological Measurement. 27, 2006, S. R63-R108. bibcode:2006PhyM...27R..63E. doi:10.1088/0967-3334/27/12/R01. Abgerufen am 5. Oktober 2011.
- P. Sun, Z. Zhang, J. Guo, Y. Shao: Fabrication of nanometer-sized electrodes and tips for scanning electrochemical microscopy. In: Analytical Chemistry. Band 73, Nr. 21, 1. November 2001, S. 5346–5351, PMID 11721940.
- Christopher J Slevin, Nicola J Gray, Julie V Macpherson, Mark A Webb, Patrick R Unwin: Fabrication and characterisation of nanometre-sized platinum electrodes for voltammetric analysis and imaging. In: Electrochemistry Communications. Band 1, Nr. 7, 1. Juli 1999, S. 282–288, doi:10.1016/S1388-2481(99)00059-4.
- Amemiya S, Bard AJ, Fan FR, Mirkin MV, Unwin PR. Annu Rev Anal Chem (Palo Alto Calif). 2008;1:95-131
- Phillip S. Dobson, John M. R. Weaver, Mark N. Holder, Patrick R. Unwin, Julie V. Macpherson: Characterization of Batch-Microfabricated Scanning Electrochemical-Atomic Force Microscopy Probes. In: Analytical Chemistry. Band 77, Nr. 2, 1. Januar 2005, S. 424–434, doi:10.1021/ac048930e.
- Fernando Cortés-Salazar, Markus Träuble, Fei Li, Jean-Marc Busnel, Anne-Laure Gassner, Mohamad Hojeij, Gunther Wittstock, Hubert H Girault. "Soft Stylus Probes for Scanning Electrochemical Microscopy" Analytical Chemistry Vol. 18, Issue 16. Date: 08/15/2009 Start Page: 6889.
- Unwin, Patrick, Jie Zhang, Christopher J. Slevin, Colin Morton, Peter Scott, David J. Walton: New Approach for Measuring Lateral Diffusion in Langmuir Monolayers by Scanning Electrochemical Microscopy (SECM): Theory and Application. In: The Journal of Physical Chemistry B. 105, 2001, S. 11120–11130. doi:10.1021/jp004592j.
- Mandler, Daniel, Tomokazue Matsue, Iva Turyan: Patterning and Characterization of Surfaces with Organic and Biological Molecules by the Scanning Electrochemical Microscope. In: Analytical Chemistry. 72, 2000, S. 3431–3435. doi:10.1021/ac000046a.
- Zhong-Qun, Dezhi Yang, Lianhuan Han, Yang Yang, Liu-Bin Zhao, Cheng Zong, Yi-Fan Huang, Dongping Zhan: Solid-State Redox Solutions: Microfabrication and Electrochemistry. In: Angewandte Chemie. 50, 2011, S. 8679–8682. doi:10.1002/anie.201103386.
- Unwin, Patrick, Julie Macpherson: Oscillatory Dissolution of an Ionic Single Crystal Surface Observed with the Scanning Electrochemical Microscope. In: The Journal of Physical Chemistry. 98, 1994, S. 11764–11770. doi:10.1021/j100096a022.
- Unwin, Patrick, Julie Macpherson: A Novel Approach to the Study of Dissolution Kinetics Using the Scanning Electrochemical Microscope: Theory and Application to Copper Sulfate Pentahydrate Dissolution in Aqueous Sulfuric Acid Solutions. In: The Journal of Physical Chemistry. 98, 1993, S. 1704–1713. doi:10.1021/j100057a026.
- Unwin, Patrick, Julie Macpherson: Scanning Electrochemical Microscope-Induced Dissolution: Theory and Experiment for Silver Chloride Dissolution Kinetics in Aqueous Solution without Supporting Electrolyte. In: The Journal of Physical Chemistry. 100, 1996, S. 19475–19483. doi:10.1021/jp9614862.
- Bard, Allen, Walsh, Fernandez: Thermodynamic Guidelines for the Design of Bimetallic Catalysts for Oxygen Electroreduction and Rapid Screening by Scanning Electrochemical Microscopy. M-Co (M: Pd, Ag, Au). In: JACS. 127, 2005, S. 357–365. doi:10.1021/ja0449729.
- Bard, Allen, Aguilar, Zoski: Scanning Electrochemical Microscopy. 46. Shielding Effects on Reversible and Quasireversible Reactions. In: Analytical Chemistry. 75, 2003, S. 2959–2966. doi:10.1021/ac034011x.
- Mallouk, Thomas, Erik Reddington, Anthony Sapienza, Bogdan Gurau, Rameshkrishnan Viswanathan S. Sarangapani, Eugene S. Smotkin: Combinatorial Electrochemistry: A Highly Parallel, Optical Screening Method for Discovery of Better Electrocatalysts. In: Science. 280, Nr. 5370, 1998, S. 1735–1737. bibcode:1998Sci...280.1735R. doi:10.1126/science.280.5370.1735.
- Liu, Biao, Susan A. Rotenberg, Michael V. Mirkin: Scanning electrochemical microscopy of living cells: Different redox activities of nonmetastatic and metastatic human breast cells. In: PNAS. 97, Nr. 18, August 2000, S. 9855–9860. bibcode:2000PNAS...97.9855L. doi:10.1073/pnas.97.18.9855.
- Pierce, David T., Patrick R. Unwin, Allen J. Bard: Scanning Electrochemical Microscopy: 17. Studies of Enzyme-Mediator Kinetics for Membrane and Surface Immobilized Glucose Oxidase. In: Anal. Chem.. 64, 1992, S. 1795–1804. doi:10.1021/ac00041a011.
- Mirkin, Michael, Yuanhua Shao: Probing Ion Transfer at the Liquid/Liquid Interface by Scanning Electrochemical Microscopy (SECM). In: Journal of Physical Chemistry B. 102, 30. Oktober 1998, S. 9915–9921. doi:10.1021/jp9828282. Abgerufen am 6. Oktober 2011.
- L.J. Thibodeaux: Environmental Chemodynamics: Movement of Chemicals in Air, Water and Soil 1996.
- Patrick Unwin, Christopher J. Slevin, Steve Ryley, David J. Walton: A New Approach for Measuring the Effect of a Monolayer on Molecular Transfer across an Air/Water Interface Using Scanning Electrochemical Microscopy. In: Langmuir. 14, Nr. 19, 1998, S. 5331–5334. doi:10.1021/la980320k.