Copolymerisation
Die Copolymerisation ist eine Sonderform einer Polyreaktion. Sie unterscheidet sich von der „einfachen“ Polyreaktion dadurch, dass statt eines Monomers (= Homopolymerisation) ein Gemisch von zwei oder mehreren chemisch unterschiedlichen Monomeren eingesetzt wird. Das Produkt der Copolymerisation ist ein Copolymer.
Allgemeines
Im Gegensatz zur einfachen Homopolymerisation, bei der nur eine einzige Monomerart zum Einsatz kommt, werden bei der Copolymerisation verschiedene Monomere gleichzeitig oder nacheinander zur Reaktion gebracht. Das Produkt der Copolymerisation ist ein Copolymer, das unterschiedliche Monomerarten in einem Molekül besitzt. Je nach der Verteilung der verschiedenen Monomerarten im Polymer unterscheidet man zwischen statistischen, alternierenden, Block- und Pfropf-Copolymeren.
Copolymerisation macht eine Vielzahl von Werkstoffen zugänglich. Durch Abstimmung der Art und Molverhältnisse der Monomeren im Polymer lassen sich viele Eigenschaften über einen weiten Bereich variieren. Eine wichtige Klasse sind die thermoplastischen Elastomere. Diese werden bei erhöhter Temperatur zu Thermoplasten und können wie diese einfach verarbeitet werden. Nach Erkalten zeigen sie wieder (gummi)elastische Eigenschaften. Auch Weichmachung (Innere Weichmachung) ist durch Copolymerisation erreichbar. Ein externer Weichmacher wird dann nicht mehr benötigt.
Reaktionskinetik
Für die Prozessführung der Synthese ist es wichtig zu wissen, welche Zusammensetzung das Copolymer haben soll. Dementsprechend müssen die Monomere eingesetzt werden. Betrachtet man zunächst die Synthese eines Copolymeren aus zwei Monomeren (für höhere Systeme gilt das Modell entsprechend). Grundsätzlich sind vier Einzelreaktionen am Kettenende eines Makromoleküls zu dessen Propagation möglich:
Aus den vier Geschwindigkeitskonstanten erstellt man nun Quotienten, die auch Copolymerisationsparameter genannt werden:
- und
Die Parameter geben die Wahrscheinlichkeit an, mit der das Monomer M oder M an ein Kettenende angelagert wird, welches eine M oder M Gruppe trägt.
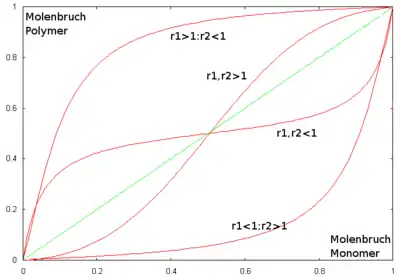
Ist z. B. , wird das Monomer 2 bevorzugt an das Kettenende 1 angelagert. Für ist es genau umgekehrt. Sind beide Parameter gleich eins, so ist keine der vier Reaktionen bevorzugt, und es kommt zu einem rein statistisch verteilten Copolymer. Aus dem Geschwindigkeitsgesetz
lassen sich die Molenbrüche im Polymer berechnen, da der Quotient von Geschwindigkeitskonstanten eine Gleichgewichtskonstante ist. Trägt man den Molenbruch einer Monomerspezies im Reaktionsansatz gegen ihren Molenbruch im Polymer auf, so erhält man das abgebildete Copolymerisationsdiagramm. Der Schnittpunkt der Kurven mit der Winkelhalbierenden (hier grün) stellt den azeotropen Punkt dar. Wird eine Reaktion unter diesen Bedingungen geführt, ist der Molenbruch einer Spezies im Reaktionsansatz genauso groß wie im resultierenden Polymer. In anderen Fällen kommt es zu einer Verschiebung des Molenbruchs während der Reaktion. Dies wird als Drift bezeichnet.
Reaktivität der Monomere
Die Reaktivität der Monomere und somit das Einbauverhalten der Monomerkomponenten in das Copolymer werden grundlegend durch zwei Faktoren dominiert.
- Resonanzeffekte
- Polaritätseffekte
Die Reaktivität eines Monomers kann durch seine kinetische Aktivität beschrieben werden. Das Copolymerisationsverhalten wird durch den Copolymerisationsparameter r bestimmt und ist folglich eine Funktion der Reaktivitäten der einzelnen Monomere.
Resonanzeffekte
Die Reaktivität eines Vinylmonomer wird durch die Struktur seines Substituenten determiniert. Resonanzstabilisierte Vinylgruppen weisen je nach Stärke der Stabilisierung eine erhöhte Aktivität des Monomers gegenüber dem Radikal auf. Stark resonanzstabilisierte Vinylmonomere sind reaktive Monomere und zugleich reaktionsträge Radikale. Dies kann zur Folge haben, dass bei einer ungeeigneten Monomerkombination (z. B.: Styrol/Vinylacetat), Homopolymerisation eintritt, da die Reaktivität der beiden Komponenten zu unterschiedlich ausgeprägt sind (r1=55, r2=0,01).
Polaritätseffekte
Einen großen Einfluss auf das Copolymerisationsverhalten hat darüber hinaus die Polarisierung der vinylischen Doppelbindung. Elektronenziehende Substituenten (EWG's) erniedrigen die Elektronendichte der Doppelbindung, wohingegen Elektronendonoren diese erhöhen. Zu den Elektronenziehenden Gruppen zählen Molekülstrukturen mit ausgeprägten −I- oder −M-Effekt, wie Ester, Ketone oder Cyanide. Den Elektronendonoren, solche mit +I- oder +M-Eigenschaften, können Alkyle oder Ether zugeordnet werden. Eine Monomerkombination von Monomeren unterschiedlicher Polarität zeigen dabei eine Neigung zur alternierenden Monomerabfolge im Copolymer. Sind die Polaritäten einander ähnlich so erfolgt eine statistische Abfolge.
Q-e-Schema
Eine semiempirische Methode der Zuordnung von Reaktivitäten Q und Polaritäten e an Monomerverbindungen wurde von Alfrey und Price beschrieben. Mit dieser Methode lassen sich Reaktivitätsverhältnisse allein aufgrund dieser beiden Parameter berechnen. Die grafische Auftragung der Reaktivitäten verschiedener Monomere im Q-e-Koordinatensystem wird auch als Q-e-Schema bezeichnet.
Die Geschwindigkeitskonstante eines Polymerwachstumsschritt wird durch die Arrhenius-Gleichung beschrieben. Die Faktoren Reaktivität Q und Polarität e sind in die Aktivierungsenergie integriert, wodurch folgende Beziehung angegeben werden kann.
Hierbei sind p1 die Reaktivität des aktiven Kettenendes, q1 die des Monomers und e1 und e2 die Polaritäten von aktiven Kettenende und Monomer. Die Reaktivitäten können dabei in den Frequenzfaktor A12 eingezogen werden, so dass man folgende Beziehung erhält.
Die Parameter Q (P) und e werden aus experimentellen Befunden (ermittelte r1, r2 Werte) bestimmt und in Relation zum Standard Styrol gesetzt, der willkürlich die Werte Q=1 und e= −0,8 zugeordnet bekommen hat.
Literatur
- B. Tieke: Makromolekulare Chemie. Wiley-VCH, 2005, ISBN 3-527-31379-6.