Carbenoide
In der Chemie ist ein Carbenoid eine reaktives Intermediat, welches die charakteristische Eigenschaft wie ein Carben besitzt,[1] oder als Quelle von Carbenen dient.[2] Hergestellt werden sie in situ aus geminalen Dihalogenverbindungen durch Ummetallierung z. B. mit Lithiumorganischen Verbindungen oder durch Metallierung durch Umsetzung mit den elementaren Metallen.
Carbenoide treten bei einer Reihe von Reaktionen als reaktive Zwischenstufe auf. Dazu gehört zum Beispiel die Simmons-Smith-Reaktion. Dabei wird das Carbenoid durch Umsetzung von Diiodmethan mit einem Zink-Kupfer-Paar erhalten. Dieses reagiert dann mit einem Alken zu einem Cyclopropan; eigentlich eine typische Reaktion eines Carbens.
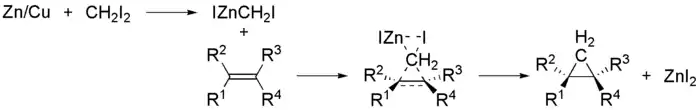 Mechanismus der Simmons-Smith-Reaktion
Mechanismus der Simmons-Smith-Reaktion
Ein weiteres Beispiel einer Reaktion von Carbenoiden ist die Fritsch-Buttenberg-Wiechell-Umlagerung. Durch Lithiierung eines geminalen Vinyldihalogenids mit Butyllithium wird das Carbenoid erhalten. Dieses lagert sich anschließend zum substituierten Acetylen (Alkin) um.
 Fritsch-Buttenberg-Wiechell-Umlagerung. Rot markiert das Carbenoid
Fritsch-Buttenberg-Wiechell-Umlagerung. Rot markiert das Carbenoid
Literatur
- Jerry March: Advanced Organic Chemistry, John Wiley & Sons, New York 1985, ISBN 0-471-88841-9.
Einzelnachweise
- Organic Chemistry, John McMurry Brooks, Cole Publishing Company, 1988, ISBN 0-534-07968-7.
- Eintrag zu carbenoids. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.C00813 – Version: 2.3..