Ramucirumab
Ramucirumab (IMC-1121B; Handelsname Cyramza) ist ein monoklonaler Antikörper, der in der Therapie von fortgeschrittenem oder metastasiertem Magenkrebs, Kolorektalkarzinom, nicht-kleinzelliges Lungenkarzinom oder Leberzellkarzinom eingesetzt wird.[1]
| Ramucirumab | ||
|---|---|---|
| ||
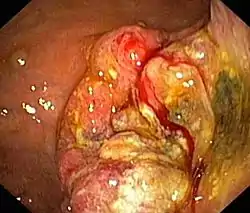
| Bereits fortgeschrittenes Stadium von Magenkrebs | ||
| Masse/Länge Primärstruktur | 1320 Aminosäuren | |
| Arzneistoffangaben | ||
| DrugBank | DB05578 | |
| Wirkstoffklasse | Monoklonaler Antikörper | |
Geschichte
Zugelassen wurde Cyramza durch die amerikanische Gesundheitsbehörde FDA im April 2014, wobei die Herstellung durch das pharmazeutische Unternehmen Eli Lilly erfolgt.[2] Die Begutachtung dieses neu entwickelten Medikaments für die Krebstherapie erfolgte dabei anhand eines beschleunigten Zulassungsverfahrens.[2]
In Deutschland (und der EU) ist Cyramza zugelassen für die Behandlung für bestimmte Patienten mit Magen-, Darm-, Lungenkrebs und Leberkrebs.[3]
Eigenschaften des Moleküls und dessen Herstellungsprozess
Ramucirumab ist ein monoklonaler Antikörper vom Typ IgG1 bestehend aus zwei schweren Ketten (engl. heavy chains; Typ γ) sowie zwei leichten Ketten (engl. light chains; Typ κ). Insgesamt besteht dieser Antikörper aus 1320 Aminosäuren und weist eine molare Masse von ca. 146,8 kDa auf. Produziert wird dieser Antikörper durch die Maus-Myelomzelllinie NS0.[4]
Wirkungsbereich
Tumoren benötigen Blutgefäße zur Versorgung mit Nährstoffen und Sauerstoff, um sich zu teilen und weiter ausbreiten zu können.[5] Vascular Endothelial Growth Factor (VEGF) ist ein wichtiges Molekül in der Entstehung und Wachstum von neuen Blutgefäßen (Angiogenese), wobei dieses Protein speziell bei Krebszellen hochreguliert wird.[6] Die Tyrosinkinase Vascular endothelial growth factor receptor 2 (VEGF R2) ist dabei ein Schlüsselmediator von VEGF-induziertem Blutgefäßwachstums. Durch die Bindung von Ramucirumab an die extrazelluläre Domäne des Rezeptors VEGF R2 wird eine Bindung der Liganden VEGF-A, VEGF-C und VEGF-D an diesen Rezeptor VEGF R2 unterbunden, wobei auch das Wachstum neuer Blutgefäße verhindert und so die Versorgung des Tumors mit Nährstoffen unterbunden wird.[4]
Verabreichung
Ramucirumab wird als Infusion in einer Dosierung von 8 mg/kg Körpergewicht in einem Zeitraum von 60 Minuten alle zwei Wochen verabreicht.[7]
Siehe auch
- Nomenklatur der monoklonalen Antikörper, Konvention zur Benennung von monoklonalen Antikörpern
Weblinks
- Öffentlicher Beurteilungsbericht (EPAR) der europäischen Arzneimittelagentur (EMA) zu: Ramucirumab
Einzelnachweise
- Cyramza. EMA, 17. September 2018, abgerufen am 5. Dezember 2019 (englisch).
- FDA approves Cyramza for stomach cancer. FDA, abgerufen am 25. August 2014 (englisch).
- Sven Siebenand: Leberkrebs: Zweitlinientherapie mit Ramucirumab möglich. Pharmazeutische Zeitung, 16. September 2019, abgerufen am 5. Dezember 2019.
- CLINICAL PHARMACOLOGY AND BIOPHARMACEUTICS REVIEW(S). FDA, abgerufen am 25. August 2014 (englisch).
- Saharinen Pipsa: VEGF and angiopoietin signaling in tumor angiogenesis and metastasis. In: Trends in Molecular Medicine. 17, Nr. 7, Juli 2011, S. 347–362. doi:10.1016/j.molmed.2011.01.015.
- Carmeliet P.: VEGF as a Key Mediator of Angiogenesis in Cancer. In: Oncology (Basel). 69, November 2005, S. 4–10. doi:10.1159/000088478.
- HIGHLIGHTS OF PRESCRIBING INFORMATION. (pdf) FDA, abgerufen am 25. August 2014 (englisch).