Nukleations-Kondensations-Modell
Das Nukleations-Kondensations-Modell (englisch: nucleation-condensation model) ist ein wissenschaftlich anerkanntes Modell zur Erklärung der Proteinfaltung. Mit dem Modell wird die Proteinfaltung über instabile Übergangszustände erklärt. Veranschaulichen lässt sich die die Problematik mithilfe einer zur Hälfte denaturierten Proteinlösung. Es leitet zur Annahme, dass das Protein zur Hälfte gefaltet sein müsste, dem ist aber nicht so. Die Lösung würde zur Hälfte vollständig gefaltete und zur Hälfte ungefaltete Proteinmoleküle beinhalten. Daraus würde man schlussfolgern, dass ein Protein nur gefaltet oder ungefaltet vorkommt, aber auf molekularer Ebene ist dies unmöglich. Zwischen dem denaturierten und dem nativen (strukturierten oder biologisch funktionsfähigen) Zustand müssen instabile Übergangszustände vorhanden sein.
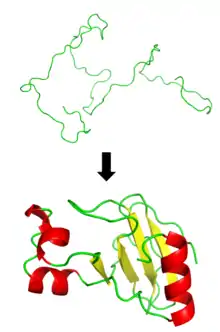
Ausgangspunkt des Modells ist die Bildung eines Proteinkerns (Nukleation eines Nucleus) als instabiler Übergangszustand, ausgehend vom denaturierten Zustand. Bestimmte Bereiche mit gewisser Strukturneigung nehmen diese Strukturen zuerst an. Zusammen bilden diese Strukturen einen Nucleus, die sich dem nativen Zustand ähneln, aber dennoch flexible Strukturen beinhalten. Dieser noch zu bildende Nucleus wird durch weitreichende Interaktionen stabilisiert, sodass der Kern sich ausbreiten kann. Die Stabilisierung des Nucleus geht dabei so schnell vonstatten, dass er nicht vollständig in den Übergangszustand überführt werden kann. Um dies wieder auszugleichen, ist die Nukleation auch mit der Kondensation gekoppelt.[1] Das heißt, die flexiblen Strukturen kondensieren vollständig und bilden die feste, native Struktur.[2][3]
Aus dem Modell geht hervor, dass bestimmte Faltungswege bevorzugt werden können. Beim Übergang vom denaturierten zum nativen Protein folgt das Protein einem allgemeinen (also dass die Übergangszustände eine Ansammlung von ähnlichen Strukturen darstellen) und nicht einem bestimmten Weg. Der energetische Ablauf für den Prozess der Proteinfaltung lässt sich in einem Faltungstrichter demonstrieren.
Literatur
- Jeremy M. Berg, Lubert Stryer, John L. Tymoczko: Stryer Biochemie. Springer-Verlag, Berlin, Heidelberg 2014, ISBN 978-3-8274-2989-6.
Einzelnachweise
- I. E. Sanchez: Protein folding transition states probed by loop extension. In: Protein Science. 17, Nr. 1, 2007, ISSN 0961-8368, S. 183–186. doi:10.1110/ps.073217708..
- A. R. Fersht, V. Daggett: Protein folding and unfolding at atomic resolution. In: Cell. Band 108, Nummer 4, Februar 2002, S. 573–582, PMID 11909527 (Review).
- Unnati Ahluwalia, Nidhi Katyal, Shashank Deep: Models of protein folding. In: Journal of Proteins and Proteomics. 3, Nr. 2, Juli–Dezember 2012, S. 85–93.