Nernstsches Verteilungsgesetz
Das Nernstsche Verteilungsgesetz (benannt nach dem Physikochemiker und Nobelpreisträger Walther Herrmann Nernst) beschreibt die Löslichkeit eines Stoffes in zwei angrenzenden Phasen. Wenn ein Stoff die Möglichkeit hat, sich zwischen zwei nicht miteinander mischbaren, stark verdünnten Phasen (z. B. einer gasförmigen und einer flüssigen Phase oder zwei flüssigen Phasen) durch Diffusion zu verteilen:
- ,
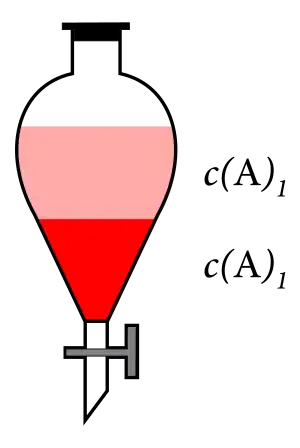
entsteht ein Verteilungsgleichgewicht, welches durch die Beziehung
beschrieben werden kann, wobei der nernstsche Verteilungskoeffizient (Gleichgewichtskonstante) und die Konzentration des Stoffes in den jeweiligen Phasen ist. Für konzentrierte Lösungen wäre jedoch statt der Konzentration die Aktivität einzusetzen.
Der Verteilungskoeffizient wird üblicherweise in Tabellen für das System Octanol/Wasser angegeben. Nernst stellte das Verteilungsgesetz 1891 auf. Es findet Anwendung beim Ausschütteln bzw. bei Extraktionen gelöster Stoffe aus Wasser mit Diethylether, Dichlormethan oder anderen organischen Lösungsmitteln, aber auch in der Pharmazie und Kosmetik bei der Ermittlung des optimalen Zusatzes von Konservierungsmitteln, die sich in Emulsionen besonders in der lipophilen Phase anreichern, aber nur in der hydrophilen Phase wirksam sind.
Verallgemeinerung zum Nernstschen Verteilungssatz
Oft ist die Kenntnis der verbleibenden Stoffmenge für das weitere Vorgehen (nochmaliges Ausschütteln) wichtig. Unter einer Verkettung von sinnvollen Annahmen kann man ein Gleichungssystem des Nernstsche Verteilungsgesetz nach der verbleibenden Stoffmenge herleiten. Je größer desto besser löst sich der Stoff in Phase und desto schlechter in Phase . Beim Ausschütteln muss die Wahl des Extraktionsmittels also nach der Größe des Verteilungskoeffizienten getroffen werden:
Da sich die Stoffmenge und Masse durch das Ausschütteln nicht verändert, ist die Summe der in Phase und Phase gelösten Stoffmengen gleich:
(Da sich nur deren Verteilung in den Phasen verändert)
Es wird nun vereinbart, die Indices 0 und 1 zu verwenden:
Durch Auflösen der Beziehung zwischen Konzentration, Stoffmenge und Volumen ergibt sich:
Es wird angenommen, dass die Stoffmenge in Phase (vor dem Schütteln) zu Beginn 0 sei:
Somit entfällt dieser Term:
Es wird ferner angenommen, dass sich das Volumen der Phase nicht ändert, da die Phase Extraktionsmittel ist:
Aus dem Umstellen des Nernstschen Verteilungsgesetzes folgt:
Durch Einsetzen erhält man den Ausdruck:
Somit ergibt sich der Nernstsche Verteilungssatz für das erste Ausschütteln zu:
Man geht davon aus, dass sich die Volumina der Phasen beim Ausschütteln nicht ändern und immer das gleiche Volumen zur Extraktion verwendet wird:
Bei n-maligem Ausschütteln ergibt sich folgende Formel:
Berechnung der extrahierten Masse
Die Konzentration (der einzelnen Phasen) umgestellt nach der Stoffmenge
kombiniert mit der Molaren Masse (des zu extrahierenden Stoffs)
ergeben einen Ausdruck, der Masse und Konzentration verknüpft:
Er kann nach der Masse aufgelöst werden:
In Kombination mit der oben hergeleiteten Gleichung ergibt sich:
Da bereits vereinbart wurde, dass sich Stoffmenge und Volumen nicht verändern, folgt für die Gesamtmasse des extrahierten Stoffs nach n-maligem Ausschütteln:
Literatur
H. Elias, S. Lorenz, G. Winnen: Das Experiment: 100 Jahre Nernstscher Verteilungssatz, Chemie in unserer Zeit, 26. Jahrg. 1992, Nr. 2, S. 70, ISSN 0009-2851