Laser-in-situ-Keratomileusis
Die Laser-in-situ-Keratomileusis (LASIK) ist eine mit einem Excimerlaser durchgeführte Augenoperation zur Korrektur optischer Fehlsichtigkeiten, die im Gegensatz zur Photorefraktiven Keratektomie (PRK) nicht an der Oberfläche, sondern ausschließlich im inneren (in-situ) Teil der Hornhaut (Stroma) durchgeführt wird. Sie stellt eine Alternative zur Korrektur einer Fehlsichtigkeit mittels Brille oder Kontaktlinse dar. Der Eingriff ist die derzeit verbreitetste Methode innerhalb der refraktiven Chirurgie.
Grundlagen

Bei diesem seit 1990 angewendeten Laserverfahren wird durch Gewebeabtrag in der Hornhaut eine Änderung der Hornhautkrümmung erreicht. Der Gewebeabtrag in der Hornhaut wird durch das Schneiden und Öffnen einer Lamelle, dem sogenannten Flap, möglich. Ein LASIK-Patient hat sehr schnell und relativ schmerzfrei scharfe Sicht, da die Operation unter der schmerzempfindlichen Hornhautoberfläche vorgenommen wird und das Epithel, im Gegensatz zu den Oberflächenbehandlungen (PRK, Trans-PRK) nicht erst nachwachsen muss. Durch den operationsbedingten Hornhauteinschnitt (flap) ergibt sich jedoch ein anders gelagertes Risikopotential als bei der oberflächlich verlaufenden PRK.
Die LASIK bietet die Chance das breiteste Spektrum der Fehlsichtigkeiten von Kurzsichtigkeit (bis -10Dpt), Weitsichtigkeit (bis +4Dpt) und Astigmatismus (bis -5Dpt) zu korrigieren, stellt aber in der Regel auch einen operativen Eingriff an einem prinzipiell gesunden Organ dar. Im besten Fall ist der verbleibende refraktive Fehler kleiner als ±0,5 Dioptrien und der Patient kann meist ohne Sehhilfen (Brille, Kontaktlinse) leben. Der unkorrigierte Visus, d. h. die Sehschärfe ohne Hilfsmittel, verbessert sich in der Regel dramatisch und erreicht idealerweise 1,0 oder mehr. Der bestkorrigierte Visus (Sehschärfe mit optimaler Brillenkorrektur) hingegen bleibt (je nach Behandlungsmethode) meist unverändert oder ändert sich geringfügig.
Historische Entwicklung der Refraktiven Chirurgie
Jahre der radialen Keratotomie (RK)
Die Operation an einem organisch gesunden Auge, welches nur einer Sehhilfe, also Brille oder Kontaktlinse bedarf, um ohne diese scharf zu sehen war keine Entwicklung, welche die Lehrstuhlinhaber von Universitäten auf den Weg brachten. Es waren die Pioniertaten von „Einzeltätern“ der praktischen angewandten Augenheilkunde, die oft vom eigenen Handicap der Abhängigkeit von der Brille getrieben waren für sich selbst eine wissenschaftlich fundierte Lösung für die Beseitigung der Fehlsichtigkeit zu finden. Die erste Publikation zu diesem Thema ist wahrscheinlich der in der damals dominierenden Wissenschaftssprache Deutsch 1885 verfasste Bericht des norwegischen Augenarztes Hjmar Schiotz[1] der in den Archiven der Augenheilkunde von der operativen Korrektur eines extremen Astigmatismus durch geschickt gewählte Hornhautschnitte berichtet. Der japanische Augenarzt Tsutomu Satō[2] griff dieses Konzept der Veränderung der Brechkraft der Hornhaut durch Hornhautschnitte wieder auf, um es nach einer Serie von enttäuschenden Eingriffen Ende der 1940er Jahre dem russischen Augenarzt Svyatoslav Fyodorov[3] zu überlassen, die Methode der radiären Keratomie[4] durch eine übermächtige Zahl an Eingriffen so zu perfektionieren, dass man mit Hilfe der von ihm entwickelten Nomogramme durch Schnitttiefe, Länge und Lage der Schnitte einigermaßen vorhersehbare Brechkraftveränderungen, im Idealfall sogar Freiheit von Brille und Kontaktlinse erreichen konnte. Diese Methode wurde später von Theo Seiler[4] bei der ersten Augenlaser-Behandlung mit dem Excimerlaser umgesetzt. Nachteilig erwiesen sich jedoch die durch die Hornhaut-Schnitte erzeugten Hornhaut-Narben, die oft nahe bis ans Zentrum der optisch wirksamen Sehachse reichten und besonders nachts bei weiter Pupille zu erheblichen Streu- und Blendungseffekten[5] führten. Auch wurde bald klar, dass mit der radialen Keratotomie operierte Patienten tageszeitliche Schwankungen der Sehschärfe hinnehmen mussten, wie auch eine Tendenz zu fortschreitender Weitsichtigkeit,[4] die gerade im Alter besonders die ohnehin eintretenden Alterssichtigkeit (Presbyopie) und damit den Bedarf an Lesebrille verstärkte. Die RK hat besonders in den USA zur weiten Verbreitung geführt.
Pionierzeit der LASIK
Zeitlich fast parallel entwickelte der spanische Augenarzt José Ignacio Barraquer[6] in Kolumbien eine chirurgische Methode, durch eine planparallele Spaltung der Hornhaut und eine intrastromale Veränderung die optischen Brechkräfte der Hornhaut umzugestalten: die sogenannte Keratomileusis (altgriechisch Κερατων Hornhaut; Μιλευσισ Formgebung). Zu dieser Zeit gab es an keiner Universität eine formale Ausbildung zur refraktiven Chirurgie, sondern die Pioniere bestellten dieses neu entstehende Feld der Augenheilkunde durch Selbststudium, selbst organisierte Workshops, klinisch experimentelles Vorgehen, Treffen auf kleinen Satelliten-Kongressen von größeren Konferenzen der Fachgruppe[7][8] oder persönlichen Tutorials. Da Instrumente wie mikrochirurgische Instrumente zum Bearbeiten der Hornhaut, wie Keratome, kalibrierbare Hornhautmesser, später auch die Excimerlaser von der in diesem Sektor aufblühenden Industrie frei verkäuflich waren, sorgten wegen der ungeregelten Ausbildung zum refraktiven Augenchirurgen systemimmanente Komplikationsmöglichkeiten der Anfangszeit zu dem zum Teil berechtigten Ruf, die refraktive Augenchirurgie sei etwas extrem Gefährliches. So entwickelte sich sehr früh eine Spaltung der Lehrmeinung in der Augenheilkunde, wobei die eine Gruppe das Zukunftspotential dieser Operationen erkannte und in den bereits vorliegenden wissenschaftlichen Erkenntnissen[9][10] die Grundlagen für einen berechtigten chirurgischen Eingriff sah, die andere Gruppe es aber als Verletzung des Berufsethos wertete, am Auge, das durch Brille oder Kontaktlinse die best-korrigierte Sehschärfe erreichte, „unnötige“ chirurgische Eingriffe vorzunehmen.[11] Bereits im Jahre 1995 kam es in Deutschland unter Federführung von Augenarzt Michael Knorz (Mannheim) zur Gründung der Kommission Refraktive Chirurgie (KRC),[12] einem Zusammenschluss der Deutschen Ophthalmologischen Gesellschaft (DOG) und des Berufsverband der Augenärzte Deutschlands (BVA), die regulativ in die Ausbildung des Laserarztes eingriff, jährliche Zertifizierungsfortbildungen anbot und seitdem jährlich Empfehlungen zur Indikation und Kontraindikation des refraktiven chirurgischen Eingriff entsprechend neuester wissenschaftlicher Erkenntnisse[13] publiziert. Am 21. September 2007 verkündete das augenärztliche Beraterteam der NASA um Steven Schallhorn, dass die Femto-LASIK als so sicher beurteilt werden konnte, dass diese Operation auch für Astronauten zugelassen werden könne.[14][15]
Internationale Kooperation
In den frühen 1990er Jahren herrschte internationale Aufbruchsstimmung in der vom Excimerlaser (EXCIted dIMer LasER) unterstützten refraktiven Hornhaut-Chirurgie. Steven Trokel[5] von der Columbia State University / New York als Kliniker, John Marshall[16] vom Moorfield’s Eye Hospital, London als Histopathologe sowie Charles Munnerlyn[17][18] (USA) als Physiker hatten die Grundlagen für die lasertechnische Anwendung des Excimerlasers und der Beschreibung seiner Wechselwirkung mit der Hornhaut gelegt. Das Jahrzehnt vorher war dominiert von mechanischen Schneidetechniken der Hornhaut, wie die Radiale Keratotomie/RK[3] von S. N. Fyodorowin der UdSSR,[19] der automatischen lamellierenden Keratotomie/ALK von Luis Ruis in Kolumbien, von Jörg Krumeich[20] in Bochum/Deutschland oder seit 1982 auch der Excimerlaser-(unterstützten)-Radialen Keratotomie (RK) von Theo Seiler in Deutschland. Der Einsatz des von IBM für die Produktion von Computer-Platinen entwickelten Excimerlasers versprach die erforderliche exponentielle Steigerung der Präzision hinein in den Mikrometer-Bereich, um die Brechkraft der Hornhaut (ca. 15 µm Dicke entsprechen ≈ 1 Dpt.) ausreichend genau vorhersagen und verändern zu können. Die von Charles Munnerlyn entwickelten Abtrags-Algorithmen am Tiermodell stellen die bis heute gültigen Grundlagen der Excimerlaser-Programmierung dar. Patentstreite zweier amerikanischer Gründer-Firmen, SUMMIT und VISX, beschäftigten noch jahrelang die amerikanischen Gerichte und endeten mit einer Millionen-Dollar-Abfindung für Steven Trokel und der Fusion der beiden Gründerfirmen (Beleg: persönliche Kommunikation Marguerite McDonald). Die erste weltweit durchgeführte Photorefraktiven Keratektomie (PRK) an einem sehenden menschlichen Auge erfolgte durch Marguerite McDonald[21] am 25. März 1988 in New Orleans / USA. Dieses Auge wurde von einer Patientin der Wissenschaft für dieses Experiment zur Verfügung gestellt, da es sowieso wegen eines malignen Melanoms entfernt werden musste. Diese historische Behandlung darf als der erste klinische Beweis gewertet werden, der die am Tiermodell erarbeitete Vorgehensweise zur Brechkraftveränderung des Auge mittels PRK am Menschen bestätigen konnte.
Die von der PRK (Photorefrakive Keratektomie) geprägten Jahre
Die bei der FDA (Food and Drug Administration/USA) eingereichten Zulassungsstudien und die ungesicherte Rechtslage für die Erstanwender der Laser-Chirurgie in den USA führte zu einem regelrechten Patienten-Tourismus aus den USA über die Grenze nach Kanada zu den Augenlaser-Pionieren Gordon Balazsi und Marc Mullie in Montreal, die, 1993 beginnend, in kurzer Zeit Verlaufsstudien zur PRK mit großer Patientenzahl auf internationalen Kongressen präsentieren konnten. Die FDA-Zulassung in den USA für die PRK erfolgte 1995 und die für die Keratom-LASIK 1998. Dies bedingte eine extrem schnellen Zunahme der Behandlungszentren mit dem Excimerlaser auch in den USA. Die eigentlichen innovativen Schritte der Weiterentwicklung der refraktiven Augenlaser-Behandlung mittels LASIK[19] erfolgten aber in dem weniger regulierten Europa. 1991 begannen José Güell[22] und Kollegen in Barcelona, Joannis Pallikaris[23][24] in Heraklion/Kreta, Lucio Buratto in Mailand/Italien, Michael Knorz in Mannheim und Theo Seiler in Dresden/Deutschland mit der Anwendung des Excimerlasers zur Beseitigung der Kurzsichtigkeit. Lucio Buratto führte Steven Slade und Stephen Brint in die Laser-Technik ein,[25] welche zurück in den USA die Zulassungsstudien bei der FDA (Federal Drug Administration) für den SUMMIT-Laser initiierten. Mit Ausnahme der Universität von Mannheim und Dresden in Deutschland, die in ihren Abteilungsleitern Michael Knorz und Theo Seiler engagierte Vertreter des neu sich entwickelnden Fachgebietes hatten, verhielten sich andere Universitäten gegenüber den Eingriffen an, im Übrigen gesunden aber nur durch abweichender Brechkraft veränderten, Augen zurückhaltend. Auch Thomas Neuhann aus München, ein später international renommierter Excimer-Laserarzt,[26] der sich über die Wundheilung der perforierenden Keratoplastik/Hornhaut-Transplantation habilitiert hatte, stand der Methode anfänglich sehr reserviert gegenüber. Einer der fortschrittlichsten Excimerlaser in Deutschland war damals der von Kristian Hohla aus Puchheim entwickelte KERACOR 116, welcher von Medizinern wie Luis Ruiz (Bogota/Kolumbien), Michael Knorz (Mannheim/Deutschland), Wolfgang Pfäffl (München/Deutschland) und Matthias Maus (Köln/Deutschland), sowie Gordon Balazsi und Marc Mullie (Montreal/Kanada) bei Bestrebungen zur Verbesserung der Excimer-Lasertechnologie angewendet wurde. Sinan Goeker (Istanbul/Türkei), der ebenfalls den gleichen Laser nutzte, verfügte damals über die ersten experimentellen klinischen Ergebnisse dieses Excimerlasers am menschlichen Auge, die für die Zulassung des Gerätes erforderlich waren. Durch die auftretenden Probleme der PRK wie reduzierte Nachtfahrtauglichkeit, Verlust der bestkorrigierten Sehschärfe durch zentrale Gewebereste („Zentrale Inseln“) oder Hornhaut-Narben-Bildung („Haze“), zu kleinen optischen Zonen sowie geringer Langzeitstabilität des Augen-Laserresultates drohte das Augenlaserverfahren in der Regenbogenpresse in Verruf zu geraten.[11][27] Eine neue Alternative stellte die aus Kolumbien kommende Technik der Keratom-LASIK nach Luis Ruiz dar, die sehr schnell von Michael Knorz in Mannheim im Rahmen der universitären Forschung etabliert werden konnte. Augenlaserchirurgen aus ganz Europa kamen nun auch nach Mannheim, um sich von Michael Knorz in die Technik einführen zu lassen. Das Auftreten von Probleme wie Schmerzen nach der Operation und „Haze“-Bildung wurden nun abgelöst durch selten beobachtete Hornhaut-Entzündung (als diffus lamellierende Keratitis), Epithel-Einwachsungen in das Hornhaut-„Flap“ oder ein irregulärer Hornhautabtrag mit dem Phänomen der bereits von der PRK bekannten zentralen Gewebe-Inselbildung beim „Broad-Beam-Laserprofil“. Emanuel Rosen[28] (London/UK), der schon früh in England zusammen mit John Marshall die PRK einzuführen versuchte, begegnete im medizinisch konservativen England noch mehr Zurückhaltung gegenüber der modernen Technik als in Deutschland herrschte, er zog sich in dieser Zeit von Excimerlaser-Behandlungen zurück.[29] Er begann erst wieder mit Augenlaserbehandlungen als unter Kristian Hohla das modernere „Flying-Spot-Laserprofil“[30] auf den Markt kam, um einem Patentstreit mit einem amerikanischen Laserhersteller aus dem Weg zu gehen.
Die LASIK-Operation gewinnt an Bedeutung
1995 führte Wolfgang Pfäffl, inspiriert von Michael Knorz aus Mannheim, der diese Technik bei Luis Ruis in Bogota kennengelernt hatte, seine erste Keratom-LASIK durch. Im gleichen Jahr begann nun auch Thomas Neuhann, der Steven Slade aus den USA als Tutor eingeladen hatte, mit der LASIK-Technik zu operieren. Die ersten Laser-assistierten Keratom-LASIKs wurden in der „free-Flap“-Technik mit dem „Automated Corneal Shaper“ von Ruiz durchgeführt. Das abgeschnittene „Flap“ wurde während der Excimerlaser-Einwirkung auf die Hornhaut beiseite gelegt und anschließend entsprechend vorher angebrachter Markierungen wieder auf die durch den Excimerlaser behandelte Hornhaut zurück verbracht. Lucio Buratto (Mailand/Italien) verlegte den Laserabtrag auf die Rückseite des „Flaps“, eine Technik, die sich wegen technischer Schwierigkeiten nicht durchsetzen konnte. Die heute übliche LASIK-Technik mit dem zurück geklappten Flap verdanken wir der eher zufälligen Entdeckung von Ioannis Pallikaris[31] aus Heraklion/Griechenland, dem bei einem geplanten „freien Flap“ das Keratom am Ende der Schnittführung hängen blieb. Da der Arbeitsbereich für den Laser genügend groß war, setzte er die Behandlung mit dem Excimerlaser fort und entdeckte dabei, dass die noch festhängende Hornhautkappe, das „Flap“ (engl. „Klappe“), viel perfekter auf dem Hornhautbett zu liegen kam, wenn es noch an seinem Scharnier (engl. „Hinge“) mit der Hornhaut verbunden blieb. In der Folgezeit wurden fast alle auf dem Markt befindlichen „Corneal Shaper“ umgebaut und mit einem Stopper versehen, um die Scharniertechnik von Pallikaris geplant durchführen zu können. Diese mechanische Schnitttechnik in den verschiedensten Varianten dominierte den Augenlaser-Markt über ein Jahrzehnt. Wegen des möglicherweise größeren Potentials eines Fehlschnittes, eines zu kleinen „Flaps“ oder irregulären „Flaps“ („Knopfloch“ „Button Hole“) durch das eingesetzte Keratom,[32] welches sich bei Saugungsverlust vom Auge lösen kann, stand auch diese Technik in der Kritik derjenigen Laseraugenärzte, die die PRK trotz ihrer Probleme als sicherere Methode propagierten, da die PRK in den USA auch die Zulassung für die Luftfahrt erhalten hatte. Die Begeisterung für die neue Technik der Keratom-LASIK verführte die Augenlaserärzte am Anfang, bei einer Fehlsichtigkeit von bis zu −25 Dpt zu lasern, eine Indikation zur Refraktiven Hornhaut-Chirurgie, die nach heutigem Kenntnisstand als Kunstfehler angesehen würde. Michael Knorz publizierte seine diesbezüglichen negativen Erfahrungen[33] und in der Folge schränkte die KRC (Kommission für Refraktive Chirurgie) in Deutschland den zuverlässigen Behandlungsbereich auf maximal -10 Dpt ein. Große Bedenken kamen auf, als das Auftreten von medizinisch induziertem Keratokonus[34] durch zu dünne Hornhaut, entweder vorbestehend oder durch die Keratom-[35] und Laserbehandlung induziert beobachtet wurden.
Maßgeschneiderte Augenlaserbehandlung mittels Wellenfront-Technologie
Das Auftreten von Komplikationen nach refraktiven Hornhaut-Eingriffen und deren Beseitigung entfachte in der optischen Industrie die Entwicklung von neuen Untersuchungsmethoden wie die Wellenfront-Analyse und eine optische Pfadmessung zur Erzeugung maßgeschneiderter Laserbehandlungen[36], die seit 1999 Thema vieler refraktiv-chirurgischer Kongresse waren. Zur Erfassung sog. "Aberrationen höherer Ordnung" werden durch ein "Linsen-Array-System" bestehend aus über 100 diagnostischen in Gitterform angeordneter Laserstrahlen von der Netzhaut reflektiert. Die Abweichungen von der Idealline in der Laufgeschwindigkeit zwischen den Einzellaserstrahlen werden gemessen und in einem rechenintensiven, aufwendigem Korrekturprogramm geglättet. So können Excimerlaser-Abtragsprofile programmiert werden, die auch dezentrierte Hornhaut-Behandlungszonen oder zu kleine optische Zonen erheblich zu bessern vermögen, wenn nicht sogar die Einschränkungen komplett beseitigen.[37]
Der Übergang von der Keratom-LASIK zur femto-LASIK
In der Entwicklung der Operationstechniken waren präzisere und möglichst dünne „Flaps“ höchst erstrebenswert, um die größtmögliche Restdicke an der Hornhaut stehen lassen zu können. Deshalb wurde die 2004 auf den Markt kommende Femtosekunden-LASIK („femto-LASIK“) schnell aufgenommen. John Marshall präsentierte 2006 auf dem 24. Kongress der ESCRS (European Society of Cataract und Refractive Surgery) die histologisch untermauerten Vorteile der Femto-LASIK und prägte den Begriff der „SBK-LASIK“.[38] Bei dieser Technik entfallen alle Gefahrenmomente der mechanischen Schnitttechnik, denn die Hornhautkappe, das „Flap“, wird unter Sicht durch die „Photodisruption“ des femto-Lasers[39] innerhalb des Gewebe erzeugt, bevor durch den Randschnitt ein Zugang zu dem Behandlungs-Ziel-Gewebe zwischen Hornhautkappe und Hornhaut-Bett möglich ist. Hier bestand nun die Problematik, wie man das über Gewebebrücken immer noch mit dem Hornhaut-Bett verbundene „Flap“ von seiner Unterlage lösen könne. Parry Binder (Los Angeles / USA), Wolfgang Pfäffl (München / Deutschland) Steven Slade (Houston/USA) und Dan Durrie (Overland Park / USA) hatten als eine der ersten Augenlaserchirurgen Zugang zu den ersten klinisch einsetzbaren Femtosekunden-Lasern des Laser-Herstellers IntraLase und beschäftigten sich intensiv wissenschaftlich mit der neuen Technik, die den Augenlaserarzt vor neue operative Herausforderungen stellte. Parry Binder, Steven Slade, Dan Durrie[40] und andere ermittelten Energieeinstellung, Schussweitenabstand der Impulse, sowie optimale Photodisruptionstiefe und zeigten die Uniformität der Hornhautkappe. John Marshall untersuchte die histologischen Gewebeeffekte und Vorteile der Gewebeeinsparung und schuf den Begriff der „SBK“ („sub-Bowman’s Keratomileusis“). Wolfgang Pfäffl und sein Team um die Technische Universität von München zeigten mittels Echtzeit-Pachymetrie[41] die Unabhängigkeit des „Femto-Flaps“ von den vielen Einstellungsparametern, die nicht mehr wie bei der Keratom-LASIK beachtet werden mussten, sowie die geringe Varianz der tatsächlich erreichten Flap-Dicke von der am femto-Laser eingestellten Ziel-Dicke des „Flaps“. Beide Gruppen beschrieben eine eigene neue Operations-Technik zur Eröffnung der im Gewebe vom Femto-Laser vorgeformten Hornhautkappe: Parry Binder die sogenannte „Hinge-Opening-Technik“[42] und Wolfgang Pfäffl die sogenannte „Flaporhexis“[43]. Michael Knorz[44] konnte in einer Studie die bessere Haftung des Femto-Flaps im Vergleich zum Keratom-Flap auf dem Hornhaut-Bett zeigen. Eine kontrollierte Vergleichsstudie zwischen dem Femtosekunden-Laser und dem mechanischen Keratom an ca. 1000 Augen aus dem Jahr 2009 beschäftigt sich mit dem Vergleich zwischen mechanischem Keratom und dem Femtosekunden-Laser[45]. In dieser Studie glaubt man nachweisen zu können, dass die postoperative Erholungszeit nach der femto-LASIK wesentlich schneller abläuft, als nach der Keratom-LASIK, wobei sich nach 3 Monaten die Ergebnisse der Sehschärfenprüfung angleichen.
Der femto-Laser als ideales Schneideinstrument in der Augenchirurgie
Die Femto-Lasertechnik hat sich als ideales Werkzeug zur kontrollierten computergesteuerten Operation an den optischen Medien des Auge erwiesen und führte zu weiteren Anwendungen wie der Femto-Katarakt-Operation und der SMILE-Operation,[46][47] einer Alternative zur LASIK-Operation. Die Bewertung dieser Methoden ist noch Teil der gegenwärtigen Wissenschaftsdiskussion.[48][49] Es zeichnet sich jedoch schon jetzt ab, dass bei der SMILE-Operation die gleichen physikalischen Grundprinzipien herrschen, bei deren Nichtbeachtung die gleichen Komplikationen drohen wie bei der femto-LASIK oder der Keratom-LASIK.[50]
Behandlungsbereich und Kontraindikationen
Die LASIK-Methode gilt indiziert für die Korrektur von:[51][52]
Die Kommission Für Refraktive Chirurgie (KRC) unterscheidet zwischen Anwendungsbereich, d. h. der Bereich, in dem das Verfahren als geeignet anzusehen ist und Komplikationen selten sind, und dem Grenzbereich, in dem das Verfahren noch angewendet werden kann, Nebenwirkungen und Komplikationsrate jedoch erwartungsgemäß höher sind. Für den Grenzbereich gelten strengere Aufklärungshinweise an den Patienten.
Anwendungsbereich
Kurzsichtigkeit bis -8,0 dpt, Weitsichtigkeit bis +3,0 dpt und Astigmatismus bis 5 Dioptrien, wobei beide Werte zusammengezählt -6,0 nicht überschreiten dürfen.
Grenzbereich
Kurzsichtigkeit bis -10,0 dpt, Weitsichtigkeit bis +4,0 dpt und Astigmatismus bis 6 Dioptrien, wobei beide Werte zusammengezählt -10,0 nicht überschreiten dürfen.
Diese Grenzen können je nach Land, Klinik und verwendetem Lasersystem ein bis zwei Dioptrien höher oder niedriger ausfallen. Die Deutsche Ophthalmologische Gesellschaft (DOG) stuft beispielsweise die LASIK nur für Kurzsichtigkeit bis −10 Dioptrien und Astigmatismus bis 3 Dioptrien als „wissenschaftlich anerkannt“ ein.[53]
Kontraindikationen sind Umstände, die eine LASIK-Behandlung verbieten oder nur unter sorgfältiger Abwägung der bestehenden Risiken zulassen, beispielsweise das Vorliegen von Anzeichen einer Hornhauterkrankung.
Wesentliche Voraussetzung für eine LASIK-Behandlung ist eine ausreichend dicke Hornhaut und das Fehlen von krankhaften Hornhautveränderungen (Indikation). Als Normalbereich der Hornhaut gilt ein Bereich von 480–600 µm. Eine zu dünne Hornhaut gilt als strenge Kontraindikation, wenn zusätzlich Risikomomente wie besonders steile Hornhaut (z. B. >49 Dpt) oder irregulärer Astigmatismus oder Vorwölbung der Rückseite der Hornhaut (subklinischer Keratokonus) vorliegen. Moderne Topographie-Geräte erzeugen mit computergestützten Rechenmodellen Wahrscheinlichkeitberechungen für das Vorliegen krankhafter Hornhautzustände. Als Grenzwert der Durchführbarkeit einer Excimer-Laseroperation gilt eine verbleibende Restdicke nach der Behandlung von mindestens 250 µm. In Deutschland soll der Operateur zusätzlich eine Reserve von 30 µm für eine eventuelle Nachkorrektur bei der Operationsplanung berücksichtigen. Berechnet wird diese Restdicke aus der Hornhautdicke abzüglich der Flap-Dicke und der maximalen Abtragstiefe. Eine LASIK sollte nicht durchgeführt werden, wenn chronisch progressive Hornhauterkrankungen vorliegen. Insbesondere bei Keratokonus verbietet sich die Behandlung, da die Hornhaut weiter geschwächt wird und sich das Krankheitsbild dramatisch verschlechtern würde. Ist die Refraktion (Augenoptik) des Patienten nicht stabil, das heißt weichen die Refraktionsbestimmungen in relativ kurzen Zeitabständen signifikant voneinander ab, sollte keine LASIK-Behandlung durchgeführt werden. Als Kontraindikationen gelten weiterhin die Augenerkrankungen Glaukom mit Gesichtsfeldschäden und symptomatischer Katarakt. Allgemeinerkrankungen, die eine LASIK-Behandlung ausschließen, sind Kollagenosen, Autoimmunkrankheiten und Wundheilungsstörungen. Schließlich sollten LASIK-Patienten mindestens 18 Jahre alt sein. Für manche Hornhauterkrankungen stellt die Augenlaserbehandlung in Form einer PTK (Phototherapeutische Keratektomie) die Therapie der Wahl dar und wird dann auch von der gesetzlichen Krankenkasse finanziell unterstützt.
Voruntersuchungen zur Augenlaser-Operation
Die Erwartungen an das Behandlungsergebnis sind von Patient zu Patient sehr unterschiedlich und sollten im Vorfeld ausgiebig mit dem behandelnden Arzt besprochen werden.[54]
Zunächst steht neben einer ausführlichen fachärztlichen Augenuntersuchung die Bestimmung der aktuellen Fehlsichtigkeit im Vordergrund. Die Refraktionsbestimmung, d. h. die Brechkraft des Brillenwertes, sollte mindestens zweimal in einem Abstand von mindestens 2 Wochen erfolgen, da Schwankungen von bis zu 0,50 dpt durchaus als normal angesehen werden. Eine genügend lange Kontaktlinsen-Pause vor der Untersuchung ist obligat zu fordern. Die Refraktionsbestimmung sollte durch einen erfahrenen Augenarzt oder einen Optometristen geschehen. Eine einzige Refraktionsbestimmung mit einem Autorefraktometer ist in jedem Fall als unzureichend einzustufen. Wünschenswert ist die Refraktionsbestimmung durch den Operateur persönlich, da er im Wesentlichen die Haftung für einen Behandlungsfehler trägt. Weiterhin muss die Hornhautdicke, meist mit Hilfe eines sogenannten Pachymeters festgestellt werden. Entscheidende Parameter für eine zum Ziel führende Augenlaseroperation ist die ideale Konstellation von Hornhaut-Dicke, Größe der geplanten optischen Zone und der zu korrigierenden Dioptrien-Zahl. Je fehlsichtiger der Patient ist oder je weiter der Durchmesser seiner Pupille bei Nacht ist, desto mehr Hornhaut muss abgetragen werden, um ein optisch perfektes Ergebnis zu erzielen. Bei einer zu dünnen Hornhaut oder nicht ausreichend groß planbaren optisch wirksamen Zone wird ein verantwortlicher Augenarzt die Operation aus Sicherheitsgründen ablehnen oder dem Patienten Abstriche von der geplanten Zielkorrektur empfehlen. Bei Abweichungen von Therapieplan oder der Überschreitung der KRC-Kriterien, die im Einzelfall erforderlich sein können, muss der Patient in Deutschland über dieses Risiko schriftlich aufgeklärt werden. Das Risiko-Profil der Augenlaseroperation ist genügend wissenschaftlich erforscht, so dass man in der Regel beide Augen an einem Tag operieren lassen kann.
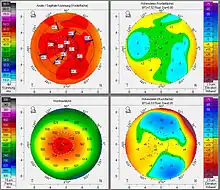
Die Voruntersuchungen dienen zum einen dazu, die korrekten Behandlungsdaten zu erfassen, zum anderen aber auch, um Kontraindikationen auszuschließen. Der Patient sollte mindestens zwei Wochen vor den Voruntersuchungen keine Kontaktlinsen tragen.
Insgesamt sollten folgende Untersuchung vor der Operation durchgeführt werden:[55]
- Bestimmung der Hornhautdicke mit einem Ultraschall-Pachymeter oder Vorderkammer-OCT
- Hornhauttopografie zur Bestimmung der Hornhautkrümmung und Erkennung von Hornhautirregularitäten
- Messung der Pupillengröße (Pupillometrie)
- Augeninnendruckmessung
- Tränenfilmbestimmung
- Allgemeine augenärztliche Untersuchung inklusive Spaltlampenuntersuchung
- Untersuchung der Netzhaut bei weit gestellter Pupille (Mydriasis/Cycloplegie)
- Anamnese
Behandlungsablauf
Zuerst wird das Auge mit Tropfen lokal betäubt und ein Lidsperrer wird eingesetzt, der das Auge weit offen hält. Mit einem Mikrokeratom (Hornhauthobel) oder einem Femtosekundenlaser (sog. Femto-LASIK) wird eine dünne Lamelle (Durchmesser etwa 8 bis 9,5 mm und Dicke zwischen 100 und 160 µm) in die Hornhaut geschnitten. Diese Lamelle (flap) wird nicht komplett abgetrennt, sondern behält eine Verbindung zur restlichen Hornhaut, die als „Scharnier“ dient. Dieses „Scharnier“ wird heute meist superior (also oben), vereinzelt aber auch noch nasal (zur Nase hin) platziert (z. T. abhängig vom Mikrokeratom) oder aber mit dem femto-Laser bei starken Astigmatismus auch als ovales Flap programmiert.
Das Mikrokeratom wie auch das Interface des Femto-Lasers besteht in der Regel aus zwei Teilen, einem Saugring zur Fixierung und einem beweglichen Schneidkopf mit einer oszillierenden Klinge bez. Laserstrahl-Austrittslinse. Während diese Vorgangs verliert das Auge vorübergehend seine Lichtwahrnehmung, da der Augeninnendruck ansteigt und der Blutfluss in den Netzhautgefäßen kurzzeitig reduziert oder unterbunden wird. Der Flap-Schnitt ist in wenigen Sekunden durchgeführt und die Sehkraft kehrt sofort zurück.
Das rechts abrufbare Video zeigt eine typische LASIK-Behandlung mit einem Mikrokeratom.
Das Auge wird von einem Lidhalter offen gehalten und die Umgebung des Auges ist steril abgedeckt. Vor dem Mikrokeratomschnitt wird die Hornhaut asymmetrisch markiert, um das Flap im Falle einer Komplikation wieder korrekt positionieren zu können. Der Saugring des Mikrokeratoms wird anschließend zentral aufs Auge platziert und das Mikrokeratom selbst eingesetzt. Mit einer schnell oszillierenden Klinge führt das Mikrokeratom die Vorwärtsbewegung aus und schneidet damit den Flap (in diesem Fall superior).
Nach dem Schnitt wird dann der Flap geöffnet und mittels Ultraschallpachymeter die restliche Hornhautdicke gemessen, um festzustellen, ob der Flap die gewünschte Dicke hatte. Bei geöffnetem Flap wird vor der eigentlichen Behandlung sichergestellt, dass die zu behandelnde Oberfläche gleichmäßig trocken ist. Wäre dies nicht der Fall, würde es, aufgrund der starken Absorption des Excimerlichts in Wasser, zu einem ungleichmäßigen Gewebeabtrag kommen.
Die Excimerlaserbehandlung selbst ist kaum wahrnehmbar, da das Licht des Excimerlasers mit seiner Wellenlänge von 193 nm unsichtbar ist. Man sieht durch das Operation-Mikroskop eine minimale Formveränderungen auf der behandelten Hornhautfläche.
Im Anschluss an den Laserabtrag wird die behandelte Fläche gespült und der Flap unter weiterem Spülen zurückgeklappt. Das gründliche Spülen ist wichtig, um eventuelle Fremdkörper (Abtragsreste, Epithelzellen, Methocelpartikel des Tupfers, Fett des Tränenfilms) aus dem Bereich zwischen Flap und Hornhaut (dem sog. Interface) zu entfernen. Mit einem kleinen Schwämmchen wird die überflüssige Flüssigkeit aus dem Interface gesaugt und der Flap glatt gestrichen. Damit ist die Behandlung beendet und der Lidsperrer kann entfernt werden.
Der Flap-Schnitt mit dem Femtosekundenlaser setzt sich immer mehr gegenüber dem mechanischen Mikrokeratom durch. Er bietet verschiedene Vorteile, insbesondere die größere Sicherheit, da der Schnitt visuell überwacht, gestoppt und nachjustiert werden kann. Wird der Laserschnitt nicht korrekt ausgeführt (z. B. Lösen des Verbindungsstückes zwischen Auge und Laser-Austrittslinse durch Saugungsverlust), kann die Behandlung je nach Fall wiederholt oder gefahrlos abgebrochen werden. Da der Laser das Gewebe mit winzigen Blasen perforiert, bleiben immer Gewebebrücken zurück, die der Arzt mit einem geeigneten Instrument trennen muss, um das Gewebe komplett zu separieren. Man kann sich das in etwa so vorstellen wie die Perforation an Briefmarken, bei der ein Kraftaufwand nötig ist, um sie zu trennen, aber die Trennung erfolgt genau an der festgelegten Stelle. Entschließt sich der Arzt also, die Behandlung abzubrechen, werden die erzeugten Bläschen vom Gewebe resorbiert und die Hornhaut ist praktisch unversehrt. Eine spezielle Technik der Hornhautkappenseparation wird Flaporhexis[56][57] genannt. Sie reduziert den mechanischen Stress der Hornhautkappe beim Separieren vom Hornhautstroma und lässt den zentralen Bereich über der Eintrittspupille frei von der Berührung mit einem Instrument. Dies stellt die ideale Voraussetzung für einen von mechanischen Instrumenten unbeeinflussten wellenfrontgeführten Abtrag mit dem Excimerlaser dar.[57][56] Eine weitere Technik der Hornhautkappenseparation ist bekannt als hinge-opening[42] („Scharnieröffner“).
Ein weiterer Vorteil ist die Präzision des Schnitts, die gewährleistet, dass der Flap mit hoher Genauigkeit die voreingestellten Dimensionen hat. Dies erlaubt das Schneiden wesentlich dünnerer Flaps (Minimum 90 µm). Die Behandlung unter Einsatz eines Femtosekundenlasers wird als Femto-LASIK bezeichnet. Sie stellt eine technisch anspruchsvollere Variante mit geringerem Gewebeverbrauch durch ein uniformes Hornhaut-Flap und damit verbunden gewöhnlich dickeren Restdicke des Hornhaut-Stromas, sowie einer stabiler gestalteten Randgeometrie dar. Bei einem sog. "Fehlschnitt" sind in der Regel keine Komplikationen zu befürchten, da das durch Photo-Disruption getrennte Gewebe in der Regel problemlos abheilt und der Schnitt nach der Abheilungszeit wiederholt werden kann.
Nach erfolgreichem Flap-Schnitt wird dieser, inklusive der Bowman´schen Basalmembran und des Epithels, zur Seite geklappt und auf dem darunter liegenden Gewebe im Hornhaut-Stroma die Laserbehandlung durchgeführt. Die Dauer der Laserbestrahlung richtet sich nach dem Ausmaß der Dpt-Korrektur und dem Behandlungsdurchmesser, liegt aber bei modernen Lasern in der Regel bei unter 30 sec. Während der Behandlung verfolgt ein sog. "Eyetracking"-System die Augenbewegungen und führt den Laserstrahl den Augenbewegungen nach. Nach Ende der Laserbehandlung wird der Flap wieder an den ursprünglichen Platz zurück geklappt, der Bereich zwischen Flap und Hornhaut gründlich gespült und der Flap sorgfältig positioniert. Ist der Arzt mit der Flap-Position zufrieden, entfernt er den Lidsperrer und der Patient kann sein Auge schließen. Das Epithel heilt am Rand des Flaps selbständig innerhalb von ein bis zwei Tagen. Ein festes Anhaften der gesamten Schnittfläche nimmt jedoch mehrere Wochen bis einige Monate in Anspruch.
Vor- und Nachteile
Vorteile der LASIK:
- Kaum Schmerzen während und nach der Operation.
- Sehr schnelle Visuserholung, das Behandlungsergebnis ist praktisch sofort nach dem Eingriff erfahrbar.
- Verglichen mit Implantaten geringes Infektionsrisiko.
- Es liegen jahrelange Erfahrungen durch weltweit Millionen von Operationen vor.
Nachteile
- Das Flap bringt verschiedene Risiken mit sich (siehe Risiken)
- Trockene Augen von durchschnittlich 6–8 Wochen, bei abnormalem Hormonstatus (Östrogen/Thyroxin) auch länger
Durch die ständige Weiterentwicklung der Technik sind ältere bzw. Langzeitstudien zur LASIK nur bedingt aussagefähig. Verbesserungen wie beispielsweise bessere Trackingsysteme und optimierte Ablationsprofile sind bei manchen Studien noch nicht eingeflossen. Moderne Behandlungsmethoden und die zunehmende Erfahrung der Operateure liefern eine hohe Vorhersagbarkeit. Etwa 85 % der Behandelten liegen im Bereich von ±0,5 Dioptrien.
In einer Studie über LASIK über ein Jahr[58] erzielten 78 % der Patienten die angestrebte Korrektur (±0,5 Dioptrien, teilweise mit zwei OPs). Nach zwölf Monaten hatten nur noch 5 % Nachtsichtprobleme. Ungefähr 94 % hatten nach diesem Jahr den gleichen oder besseren unkorrigierten Visus. Sehr ausführliche Studienergebnisse präsentiert die amerikanische Food and Drug Administration (FDA) auf ihrer Webseite.[59] Diese Studien werden im Rahmen der Zulassungsverfahren für refraktive Lasergeräte durchgeführt und gelten als sehr zuverlässig. Sie werden streng überwacht und an mehreren Kliniken parallel durchgeführt.
Risiken
Wie bei jedem operativen Eingriff gibt es auch bei der LASIK eine Reihe von Risiken. Die Art und Häufigkeit des Auftretens hängen unter anderem von der Erfahrung des Operateurs, der Höhe der Korrektur, der verwendeten Laser- oder Operations-Technik und individueller patientenbezogener Einflussfaktoren ab.
Allgemeine Risiken, die sowohl bei der LASIK, aber auch bei jeder anderen Art von refraktiver Chirurgie bestehen, sind Einschränkungen des Dämmerungs- und Nachtsehens bei zu kleiner erreichter optischer Zone durch reduzierte Kontrastsensitivität, Glare (Glanzeffekte) und Halogone (Lichthöfe).[60][5] Auftreten können außerdem kurz- bis langfristige Über- oder Unterkorrekturen sowie eine Verringerung der Sehschärfe mit optimaler Brillenkorrektur (sog. bestkorrigierter Visus). Infektionen am Auge sind selten, aber möglich und können in der Regel bei sorgfältiger postoperativer Betreuung gut behandelt werden.
Das Risiko von Sehbeeinträchtigungen nach einer LASIK-Behandlung hängt auch von individuellen Risikofaktoren (etwa der Dioptrienzahl, flache Hornhaut, Pupillengröße[58]) ab.[61] Außerdem hat die Erfahrung des Operateurs einen gravierenden Einfluss auf die Komplikationsrate. Eine Studie aus dem Jahr 1998 vergleicht die intraoperative Komplikationsrate der ersten 200 Behandlungen eines Operateurs mit der der folgenden 4800 Behandlungen. Bei den ersten 200 Behandlungen liegt die Rate bei 4,5 %, bei den weiteren Behandlungen nur bei 0,87 %.[62]
Ein gewisses Risiko besteht in der strukturellen Schwächung der Hornhaut nach dem Gewebsabtrag. Diese Schwächung und der ständig auf die Hornhaut einwirkende Augeninnendruck können zu einer Vorwölbung der Hornhaut führen (Keratektasie). Das Risiko dafür steigt mit abnehmender Restdicke der Hornhaut nach der Behandlung. Als Mindestwert für die Restdicke gelten 250 µm. Die Restdicke berechnet sich aus der zentralen Hornhautdicke abzüglich der Flapdicke und des zentralen Gewebeabtrags. Post-LASIK Keratektasie ist eine Langzeitkomplikation, die mit einer Latenzzeit von bis zu 10 Jahren auftreten kann. Die Häufigkeit dieser schweren, sehbeeinträchtigenden Komplikation wird mit ca. 0,6 % und 0,9 % bzw. bis zu 2,5 % bei höheren Kurzsichtigkeiten angegeben.[63][64][65]
Insbesondere durch das Schneiden des Flaps bringt die LASIK-Methode eine Reihe von Risiken[51] mit sich. In den ersten Tagen nach der Behandlung kann es zu einem Missempfinden an der Hornhaut kommen. Sehr häufig, in 15–20 % der Fälle, treten trockene Augen in den ersten Wochen oder Monaten nach der Behandlung auf. Die Ursache für trockene Augen liegt im Durchtrennen von Hornhautnerven durch den Flapschnitt. Die durchtrennten Nerven können nicht mehr die Austrocknung der Hornhautoberfläche erkennen und Tränenproduktion und Lidschlagfrequenz werden reduziert. Für Patienten mit chronischem trockenen Auge erhöht sich die Wahrscheinlichkeit einer Wiederverschlechterung.[66]
Das Schneiden des Flaps stellt insbesondere bei der Benutzung eines Mikrokeratoms ein ernst zu nehmendes Risiko dar. Die gewünschte Form und Größe des Flaps wird unter Umständen nicht erreicht und in seltenen Fällen kann es auch zu unvollständigen oder durchbrochenen Flaps (Hemi-Flap oder Knopfloch-Flap) kommen. Ein weiteres Risiko insbesondere des Keratom-Flaps ist das Einwachsen von Epithelzellen vom Randschnitt unter den Flap. Diese führen zu Trübungen im betroffenen Areal, sind aber vom Arzt relativ einfach zu entfernen. Der Flap kann nach der Behandlung durch starke äußere Einflüsse verschoben, oder gar abgetrennt werden. Eine solche Gefahr besteht insbesondere bei Sport- oder Autounfällen. Schließlich besteht bei jeder Augenlaser-Operation die Gefahr einer Ektasie und zwar möglicherweise bei der Keratom-LASIK in höherem Maße als bei der PRK, da die Hornhaut in einem tiefer liegendem Gewebeabschnitt geschwächt wird. Generell wünschenswert wäre deshalb der routinemäßige Einsatz der sog. Online-Pachymetrie die während der laufenden Excimerlaser-Einwirkung auf die Hornhaut dessen Abtrag in Echtzeit misst, um so zu vermeiden, dass der Excimer versehentlich zu tief in die Hornhaut eindringt und die kritischen Grenzwerte unterschreitet.[56][26]
Da die ersten LASIK-Behandlungen erst 1990 durchgeführt wurden, gibt es inzwischen längerfristige Erkenntnisse zu deren eventuellen Spätfolgen.[27][67] Bei etwa < 1 % aller Patienten von LASIK kommt es zu Komplikationen während der OP. Der Flap hält nach der Operation größtenteils über adhäsive Kräfte. Das Anheben des Flaps ist selbst noch nach sieben Jahren möglich.[68] Das Flap erweist sich als äußerst stabil. Absolute Raritäten sind Dislokationen mit nur geringer äußerer Einwirkung (Reiben am Auge, Kontaktlinsen). Möglich sind diese durch Sportverletzungen (etwa Squash-Ball oder Gummiexpander), Kontakt mit den Krallen von Haustieren oder Autounfälle mit Airbag-Auslösung. Nur bei korrekter und zeitnaher Revision durch einen Spezialisten[69][70] kann im Unglücksfall wieder ein akzeptabler Visus hergestellt werden.
Qualitätsnachweis
Der objektive Nachweis von Qualität ist für Patienten sehr wichtig. Es gibt verschiedene Zertifikate, die im Gesundheitswesen angewendet werden.
QM-Zertifikat nach ISO 9001
Das ISO-9001-Zertifikat ist ein reines prozessorientiertes Qualitätsmanagementsiegel, welches branchenübergreifend vergeben wird. Es reflektiert Prozessqualität und sagt nichts über die Qualität der medizinischen Behandlung oder den technischen Stand der eingesetzten Instrumente aus.
LASIK-TÜV (2006–2017)
Speziell für Augenlaserzentren gab es von 2006 bis 2017 den sogenannten LASIK-TÜV, der auf dem ISO-9001:2000-Zertifikat aufbaute. Er wurde vom TÜV SÜD angeboten und wurde in Zusammenarbeit mit der Kommission Refraktive Chirurgie (KRC), dem Verband der Spezialkliniken für Augenlaser und Refraktive Chirurgie (VSDAR e. V.) und dem Berufsverband der Ophthalmochirurgen (BDOC) entwickelt. Im Gegensatz zum ISO-9001:2000-Zertifikat prüfte der LASIK-TÜV nicht nur die Prozessqualität, sondern auch die Dienstleistungs- und Ergebnisqualität. Konkret wurden folgende Aspekte geprüft:[71][72]
- Qualifikation und Erfahrung der Mitarbeiter und Ärzte,
- technische Ausstattung der Einrichtung,
- Hygiene-Standards der Einrichtung,
- Behandlungsergebnisse,
- Patientenzufriedenheit.
Die Erteilung von TÜV Zertifikaten für LASIK-Anbieter wurde zum Januar 2017 eingestellt. Seitdem dürfen die entsprechenden Prüfzeichen von den Kliniken nicht mehr verwendet werden.[73]
Alternativen
Operationsmethoden mit einer geringeren Häufigkeit des Auftretens von Flap-bedingten Komplikationen sind:
- Femtosekunden-Lentikel-Extraktion – der Flap wird mittels Laser geschnitten
- Small Incision Lenticule Extraction – nur ein kleiner Schnitt mittels Laser von 2 bis 4 mm Länge ist erforderlich
Literatur
- Theo Seiler: Refraktive Chirurgie der Hornhaut. Georg Thieme Verlag, Stuttgart 2000, ISBN 3-13-118071-4.
- Berthold Graf: Ein Leben ohne Brille und Kontaktlinsen – Augenlaser und andere Alternativen. Baltic Sea Press, Rostock 2009, ISBN 978-3-942129-14-5.
- Thomas Kohnen: Refraktive Chirurgie. Springer, Berlin 2010, ISBN 978-3-642-05405-1.
- Irmgard Huber, Wolfgang Lackner, Wolfgang Pfäffl: Augenlaser – Die Erfolgstherapie bei Fehlsichtigkeit. 2. Auflage. Schlütersche Verlagsgesellschaft, Hannover 2005, ISBN 3-517-06202-2.
Weblinks
Einzelnachweise
- H. Schiotz: Ein Fall von hochgradigem Hornhautastigmatismus nach Starextraktion. Besserung auf operativem Wege. In: Arch Augenheilkd. 15, 1885, S. 178–181.
- T. Sato, K. Akiyama, H. Shibata: A new surgical approach to myopia. In: Am J Ophthalmol. 36(6 1), Jun 1953, S. 823–829.
- S. N. Fjodorow, V. V. Durnev: Operation of dosaged dissection of corneal circular ligament in cases of myopia of mild degree. In: Ann Ophthalmol. 11(12), Dec 1979, S. 1885–1890.
- T. Seiler: Recent developments in refractive corneal surgery. In: Curr Opin Ophthalmol. Band 3, Nr. 4, 1992, S. 482–487.
- G. J. Florakis, D. A. Jewelewicz, N. I. Fan, S. L. Trokel: Night vision testing in unoperated eyes. In: J Refract Surg. Band 12, Nr. 2, 1996, S. 311–312.
- J. I. Barraquer: Queratoplastia Refractiva. In: Estudios e Informaciones Oftalomológicas. 10, 1949, S. 1–21.
- H. E. Kaufman, M. B. McDonald: Refractive surgery for aphakia and myopia. In: Trans Ophthalmol Soc U K. 1985, 104(Pt 1), S, 43–47
- W. Pfäffl, M. R. Pertzsch, M. Ulmann: Die Korrektur der Myopie größer -8,0dpt mittels Photoablativer Keratektomie (PRK) nach 2 Jahren. 10. Kongress der Deutschen Ophthalmochirurgen (DOC), Internationales Symposium, 12.–15. Juni 1997.
- P. S. Binder: Analysis of ectasia after laser in situ keratomileusis: risk factors. In: Journal of Cataract and Refractive Surgery. 33, 2007, S. 1530–1538.
- K. D. Solomon, L. E. Fernández de Castro, H. P. Sandoval, J. M. Biber, B. Groat, K. D. Neff, M. S. Ying, J. W. French, E. D. Donnenfeld, R. L. Lindstrom; Joint LASIK Study Task Force: LASIK world literature review: quality of life and patient satisfaction. In: Ophthalmology. 116(4), Apr 2009, S. 691–701. doi:10.1016/j.ophtha.2008.12.037. Review. PMID 19344821
- Veronika Hackenbroch: Die Hornhaut ist für eine Lasik nicht geeignet. In: Spiegel Online. 12. November 2008 (Kritikergespräch).
- Kurzübersicht über die Methoden der refraktiven Chirurgie. Kommission Refraktive Chirurgie (KRC), 2010; abgerufen am 3. November 2010.
- Thomas Kohnen, Anja Strenger, Oliver K. Klaproth: Basiswissen refraktive Chirurgie. Korrektur von Refraktionsfehlern mit modernen chirurgischen Verfahren. In: Deutsches Ärzteblatt. Jg. 1051, Nr. 9129, 2008, S. 163–177 (PDF).
- P. F. Stanley, D. J. Tanzer, S. C. Schallhorn: Laser refractive surgery in the United States Navy. In: Curr Opin Ophthalmol. 2008 Jul, 19(4), S. 321–324. doi:10.1097/ICU.0b013e3283009ee3. Review. PMID 18545015
- Refractive surgery program policy changes (englisch) U.S. Air Force. 24. Mai 2007. Abgerufen am 12. Juli 2019.
- D. P. O’Brart, C. P. Lohmann, F. W. Fitzke, G. Klonos, M. C. Corbett, M. G. Kerr-Muir, J. Marshall: Discrimination between the origins and functional implications of haze and halo at night after photorefractive keratectomy. In: J Refract Corneal Surg. Band 10, Nr. 2, 1994, S. 281.
- A. W. Chang, A. C. Tsang, J. E. Contreras, P. D. Huynh, C. J. Calvano, T. C. Crnic-Rein, E. H. Thall: Corneal tissue ablation depth and the Munnerlyn formula. In: J Cataract Refract Surg. Band 29, Nr. 6, 2003, S. 1204–1210.
- C. R. Munnerlyn, S. J. Koons, J. Marshall: Photorefractive keratecomy: a technique for laser refractive surgery. In: Journal of Refractive Surgery. Band 14, 1988, S. 46–52.
- Dan Z. Reinstein, Timothy J. Archer, Marine Gobbe: The History of LASIK. In: Journal of Refractive Surgery. Band 28, Nr. 4, 1. April 2012, ISSN 1081-597X, S. 291–298, doi:10.3928/1081597x-20120229-01 (healio.com [abgerufen am 4. November 2018]).
- G. I. Duncker, J. Krumeich, F. Wilhelm, T. Bredehorn: Lamellar Keratoplasty. In: Klin Monbl Augenheilkd. Band 221, Nr. 1, 2004, S. 14–23.
- R. W. Beuerman, M. B. McDonald, D. Zhang, R. J. Varnell, H. W. Thompson: Diclofenac sodium attenuates neural activity after photorefractive keratectomy in rabbits. In: J Refract Surg. Band 12, Nr. 7, 1996, S. 783–791.
- J. L. Güell: Time-expanding options in laser corneal refractive surgery. In: Br J Ophthalmol. Band 97, Nr. 8, 2013, S. 951–952.
- I. G. Pallikaris, D. S. Siganos: Excimer laser in situ keratomileusis and photorefractive keratectomy for correction of high myopia. In: J Refract Corneal Surg. Band 10, Nr. 5, 1994, S. 498–510.
- V. J. Katsanevaki, Kalyvianaki, D. S. Kavroulaki, I. G. Pallikaris: MI Epipolis laser in-situ keratomileusis: an evolving surface ablation procedure for refractive corrections. In: Current Opinions of Ophthalmology. 4. Auflage. Nr. 17, 2006, S. 389–393.
- Larkin Howard: A proud heritage. In: Eurotimes. Band 15, Nr. 6, 2010, S. 4–6.
- I. M. Neuhann, B. A. Lege, M. Bauer, J. M. Hassel, A. Hilger, T. F. Neuhann: Online optical coherence pachymetry as a safety measure for laser in situ keratomileusis treatment in 1859 cases. In: J Cataract Refract Surg. Band 34, Nr. 8, 2008, S. 1273–1279.
- ARD-Magazin Monitor vom 9. Oktober 2003.
- E. S. Rosen: LASIK mania. In: J Cataract Refract Surg. Band 26, Nr. 3, 2000, S. 303–304.
- E. S. Rosen: Uncannily prescient. In: J Cataract Refract Surg. Band 10, Nr. 28, 2002, S. 1717–1718.
- T. Fiore, F. Carones, R. Brancato: Broad beam vs. flying spot excimer laser: refractive and videokeratographic outcomes of two different ablation profiles after photorefractive keratectomy. In: J Refract Surg. Band 17, Nr. 5, 2001, S. 534–541.
- G. D. Kymionis, N. S. Tsiklis, N. Astyrakakis, A. I. Pallikaris, S. I. Panagopoulou, I. G. Pallikaris: Eleven-year follow-up of laser in situ keratomileusis. In: Journal of Cataract and Refractive Surgery. Band 33, Nr. 2, 2007, S. 191–196.
- R. D. Stulting, J. D. Carr, K. P. Thompson, G. O. Waring 3rd, W. M. Wiley, J. G. Walker: Complications of laser in situ keratomileusis for the correction of myopia. In: Ophthalmology. Band 106, Nr. 1, 1999, S. 13–20.
- M. C. Knorz, B. Wiesinger, A. Liermann, V. Seiberth, H. Liesenhoff: Laser in situ keratomileusis for moderate and high myopia and myopic astigmatism. In: Ophthalmology. Band 105, Nr. 5, 1998, S. 932–940.
- P. S. Binder: Analysis of ectasia after laser in situ keratomileusis: risk factors. In: Journal of Cataract and Refractive Surgery. Band 33, 2007, S. 1530–1538.
- K. D. Solomon, E. Donnenfeld, H. P. Sandoval, O. Al Sarraf, T. J. Kasper, M. P. Holzer, E. H. Slate, D. T. Vroman: Flap Thickness Study Group Flap thickness accuracy: comparison of 6 microkeratome models. In: J Cataract Refract Surg. Band 30, Nr. 5, 2004, S. 964–977.
- M. Mrochen, M. Kaemmerer, T. Seiler: Wavefront-guided laser in situ keratomileusis: early results in three eyes. Band 16, Nr. 2. J Refract Surg., 2000, S. 116–121.
- Irmgard Huber, Wolfgang Lackner, Wolfgang Pfäffl: Augenlaser - Erfolgstherapie bei Fehlsichtigkeit. 2. Auflage. Schlütersche Verlagsgesellschaft, Hannover 2005, S. 46–49.
- John Marshall: Wound healing and biomechanics of corneal flap creation. In: ESCRS (Hrsg.): XXIV Congress of the ESCRS. London 2006.
- I. Ratkay-Traub u. a.: Ultra-short pulse (femtosecond) laser surgery: initial use in LASIK flap creation. In: Ophthalmology clinics of North America. Band 14, Nr. 2, 2001, S. 347–355.
- S. G. Slade, D. S. Durrie, P. S. Binder: A prospective, contralateral eye study comparing thin-flap LASIK (sub-Bowman keratomileusis) with photorefractive keratectomy. In: Ophthalmology. Band 116, Nr. 6, 2009, S. 1075–1082.
- W. A. Pfaeffl, M. Kunze, U. Zenk, M. B. Pfaeffl, T. Schuster, C. Lohmann: Predictive factors of femtosecond laser flap thickness measured by online optical coherence pachymetry subtraction in sub-Bowman keratomileusis. In: Journal of Cataract and Refractive Surgery. Band 34, Nummer 11, November 2008, S. 1872–1880. doi:10.1016/j.jcrs.2008.07.017. PMID 19006732
- P. S. Binder: One thousand consecutive IntraLase laser in situ keratomileusis flaps. In: Journal of Cataract and Refractive Surgery. Band 32, Nr. 6, 2006, S. 962–969.
- W. A. Pfaeffl: Opening the Femtosecond Laser Flap. In: Cataract & Refractive Surgery Today. 6. Auflage. Nr. 1, 2006, S. 22–23.
- M. C. Knorz, U. Vossmerbaeumer: Comparison of flap adhesion strength using the Amadeus microkeratome and the IntraLase iFS femtosecond laser in rabbits. In: Journal of Refractive Surgery. Band 24, Nr. 9, 2008, S. 875-788.
- M. Tanna, S. C. Schallhorn, K. A. Hettinger: Femtosecond laser versus mechanical microkeratome: a retrospective comparison of visual outcomes at 3 months. Band 25. Journal of Refractive Surgery, 2009, S. 668–671.
- W. Sekundo, K. S. Kunert, M. Blum: Small incision corneal refractive surgery using the small incision lenticule extraction (SMILE) procedure for the correction of myopia and myopic astigmatism: results of a 6 month prospective study. In: British Journal of Ophthalmology. Band 95, Nr. 3, 2011, S. 335–339.
- M. Blum, K Täubig, C. Gruhn, W. Sekundo, K. S. Kunert: Five-year results of Small Incision Lenticule Extraction (ReLEx SMILE). In: British Journal of Ophthalmology. Band 100, Nr. 9, 2016, S. 1192–1195.
- D. Z. Reinstein, T. J. Archer, J. B. Randleman: Mathematical model to compare the relative tensile strength of the cornea after PRK, LASIK, and small incision lenticule extraction. In: Journal of Refractive Surgery. Band 29, Nr. 7, 2013, S. 454–460.
- M. Moshirfar, J. C. Albarracin, J. D. Desautels, O. C. Birdsong, S. H. Linn, P. C. Hoopes Sr.: Ectasia following small-incision lenticule extraction (SMILE): a review of the literature. In: Clinical Ophthalmolology. Band 15, Nr. 11, 2017, S. 1683–1688.
- J. B. Randleman: Ectasia After Corneal Refractive Surgery: Nothing to SMILE About. In: Journal of Refractive Surgery. Band 32, Nr. 7, 2016, S. 434–435.
- Thomas Kohnen, Anja Strenger, Oliver K. Klaproth: Basiswissen refraktive Chirurgie. Korrektur von Refraktionsfehlern mit modernen chirurgischen Verfahren. In: Deutsches Ärzteblatt. Jg. 1051, Nr. 9129, 2008, S. 163–177. dgii.org (Memento vom 6. Juli 2010 im Internet Archive) (PDF)
- Kurzübersicht über die Methoden der refraktiven Chirurgie. (Nicht mehr online verfügbar.) Kommission Refraktive Chirurgie (KRC), 2010, archiviert vom Original am 4. März 2016; abgerufen am 1. Dezember 2018. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- Patienteninformation zur Laser in situ Keratomileusis (LASIK). (Nicht mehr online verfügbar.) Kommission Refraktive Chirurgie (KRC), 2010, archiviert vom Original am 27. November 2010; abgerufen am 3. November 2010. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- Untersuchungen und Maßnahmen, die vor einer Operation ergriffen werden müssen. LasikVerzeichnis, redaktionelle Informationen über Augenoperationen
- notwendige Untersuchungen bevor die Fehlsichtigkeit korrigiert werden kann (Memento vom 6. Januar 2013 im Webarchiv archive.today). Universitätsklinikum Carl Gustav Carus Dresden an der Technischen Universität Dresden.
- W. A. Pfaeffl, M. Kunze, U. Zenk, M. B. Pfaeffl, T. Schuster, C. Lohmann: Predictive factors of femtosecond laser flap thickness measured by online optical coherence pachymetry subtraction in sub-Bowman keratomileusis. In: Journal of Cataract and Refractive Surgery. Band 34, Nummer 11, November 2008, S. 1872–1880. doi:10.1016/j.jcrs.2008.07.017. PMID 19006732
- S. E. Wilson, M. R. Santhiago: Flaporhexis: Rapid and effective technique to limit epithelial ingrowth after LASIK enhancement. In: Journal of Cataract and Refractive Surgery. [elektronische Veröffentlichung vor dem Druck] November 2011. doi:10.1016/j.jcrs.2011.10.015. PMID 22082751
- Mihai Pop, Yves Payette: Risk Factors for Night Vision Complaints after LASIK for Myopia. In: Ophthalmology. 111, 2004, S. 3–10, arcor.de/pinnipedii (PDF).
- FDA-Approved Lasers for LASIK. Food and Drug Administration, 27. November 2009.
- Simulator für Dämmerungs- und Nachtsehen nach LASIK in Abhängigkeit von Dioptrienzahl und Pupillendurchmesser. 28. April 2010.
- Individuelle Risikofaktoren für Halos, Kontrastverlust, Blendung, Starburst nach LASIK. operationauge.de, 11. März 2010.
- J. S. Vidaurri-Leal: Complications in 5000 LASIK procedures. In: Group RSSI (Hrsg.): Refractive Surgery. 1998, S. 61–64.
- PS. Binder: Analysis of ectasia after laser in situ keratomileusis: risk factors. In: Journal of Cataract and Refractive Surgery. 33, 2007, S. 1530–1538.
- L. Spadea u. a.: Corneal Crosslinking for Keratectasia after Laser in situ Keratomileusis: A Review of the Literature. In: J Kerat Ect Cor Dis. 2, 2013, S. 113–120.
- J. L. Alio u. a.: Laser in situ keratomileusis for −6.00 to −18.00 dioptres of myopia and up to −5.00 dioptres of astigmatism: 15-years follow-up. In: Journal of Cataract and Refractive Surgery. 41, 2015, S. 33–40.
- Julie Albietz u. a.: Chronic dry eye and regression after laser in situ keratomileusis for myopia. In: Journal of Cataract & Refractive Surgery. Volume 30, Issue 3, S. 675–684, March 2004 (jcrsjournal.org).
- Veronika Hackenbroch: Die Hornhaut ist für eine Lasik nicht geeignet. In: Spiegel Online. 12. November 2008 (Kritikergespräch).
- Sunil Shah, Vinod Kumar: Has LASEK superseded LASIK? In: Optometry Today. 6/2003, S. 22–25. laseroogchirurgie.com (PDF).
- Quentin Franklin u. a.: Late Traumatic Flap Displacement after LASIK. In: Military Medicine. Nr. 169, 2004, S. 334–336, home.arcor.de/pinnipedii (PDF).
- T. H. Tsai, K. L. Peng, C. J. Lin: Traumatic corneal flap displacement after laser in situ keratomileusis (LASIK). In: Int Med Case Rep J. Band 10, Nr. 19, April 2017, S. 143–148.
- TÜV Süd: Liste zertifizierter Kliniken. Abgerufen am 6. Dezember 2010.
- Das Gütesiegel LASIK TÜV. (Nicht mehr online verfügbar.) Archiviert vom Original am 6. März 2010; abgerufen am 3. März 2010. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- TÜV-Süd – Der Standard LASIK-TÜV SÜD wurde eingestellt