Elektroneneinfangdetektor
Ein Elektroneneinfangdetektor (kurz ECD für englisch electron capture detector) ist ein Bauteil eines Gaschromatographie-Geräts. Er kommt vor allem dann zur Verwendung, wenn beispielsweise im Rahmen der Umwelt- oder Spurenanalytik schwefelhaltige, nitrierte oder halogenierte Verbindungen nachgewiesen und quantifiziert werden sollen.
Technikgeschichte
.jpg.webp)
Der ECD wurde 1957 von James E. Lovelock[1][2] entwickelt. Erst mit dem ECD wurde es möglich, chlorierte Umweltschadstoffe wie Polychlorierte Biphenyle (PCB) und chlorierte Pestizide wie DDT durch Gaschromatographie empfindlich nachzuweisen.
Funktionsprinzip
Der Detektor besteht aus einer Ionisationskammer mit einer Kathode und einer Anode, sowie über einen Einlass und einen Auslass für den Gasstrom.
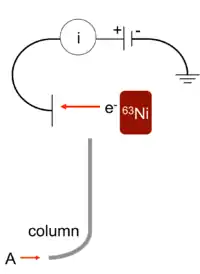
Als β-Strahler dient eine radioaktive Quelle in Form einer dünnen Metallfolie, die mit dem radioaktiven Nickelisotop 63Ni beschichtet ist. Die Elektronenquelle stellt gleichzeitig die Kathode dar. Der β-Zerfall führt zur Emission von Primärelektronen, die mit den N2-Molekülen des Trägergases kollidieren. Es entstehen positiv geladene N2-Molekülionen und freie Sekundärelektronen. Durch Anlegen einer Spannung entsteht ein elektrisches Feld, durch das sich die freien Sekundärelektronen zur Anode bewegen. Den auf diese Weise entstehenden Strom von wenigen Nanoampere (nA) bezeichnet man als Ionisationsgrundstrom.
Wird im Trägergas eine Probensubstanz mit hoher Elektronenaffinität mitgeführt, dann wird von diesem Stoff ein Teil der freien Elektronen eingefangen, wodurch sich der Ionisationsgrundstrom verringert. Diese Verringerung stellt das Detektorsignal dar. Das bedeutet in der Praxis, dass der ECD auf Substanzen reagiert, die eine Affinität zu Elektronen haben (z. B. halogenierte Verbindungen so wie die meisten persistenten Umweltgifte).
Da diese klassische Betriebsart mit dem Nachteil eines geringen linearen Bereichs behaftet ist, arbeiten moderne Geräte aufwendiger. Dabei wird ein Spannungsimpuls in einer variablen Frequenz angelegt. Während des Moments (0,5 bis 1 µs), in dem die Spannung anliegt, werden die Elektronen, die nicht mit den Substanzen des Trägergasstrom reagiert haben, von der Anode eingesammelt. Die Pulszeit ist so kurz gewählt, dass die durch Aufnahme von Elektronen entstandenen schweren Ionen die Anode nicht erreichen können. Die Frequenz wird nicht konstant gehalten, sondern zielt darauf ab, eine immer gleich bleibende Stromstärke zu erzeugen. Werden dem Gerät also eine große Anzahl an elektrophilen Molekülen über den Gasstrom zugeführt, erhöht sich zum Ausgleich die Frequenz, da weniger Elektronen die Anode erreichen und damit die Stromstärke abnimmt. Als Detektorsignal dient jetzt nicht mehr die Verringerung des Ionisationsgrundstromes, sondern die Frequenz, mit der die Spannung angelegt wird, um die Stromstärke konstant zu halten. Die Impulsfrequenz verhält sich damit proportional zur Konzentration der elektroneneinfangenden Moleküle.
Durch die Variation der pulsfreien Zeit ist die Zahl der freien Elektronen weitgehend konstant. Das bedeutet, dass auch bei hohen Analyt-Konzentrationen genügend Elektronen zur Ionisation bereitstehen. Die Elektronenzahl passt sich der Analytkonzentration an, wodurch der lineare Bereich deutlich erweitert wird.
Detektorempfindlichkeit
Der ECD übertrifft bezüglich Nachweisgrenzen einen Flammenionisationsdetektor (FID) um mehrere Größenordnungen. Zu erwartende Detektorempfindlichkeiten für verschiedene Klassen von organischen Verbindungen sind:[3][4]
| Chemische Gruppe | Relative Empfindlichkeit (zum FID) |
|---|---|
| Kohlenwasserstoffe | 1 |
| Ether, Ester | 10 |
| Aliphatische Alkohole, Ketone, Amine, | 100 |
| Mono-Cl- u. Mono-F-Verbindungen, Mono-Br-, Di-Cl- u. Di-F-Verbindungen | 1000 |
| Aldehyde und Tri-Cl-Verbindungen | 104 |
| Mono-I-, Di-Br- und Nitroverbindungen | 105 |
| Di-I-, Tri-Br-, Poly-Cl und Poly-F-Verbindungen | 106 |
Die Tabelle liefert nur angenäherte Werte. Die Empfindlichkeit variiert abhängig von der Verbindungsstruktur stark innerhalb jeder Gruppe der Verbindungen.
Einzelnachweise
- J.E. Lovelock: A Sensitive Detector for Gas Chromatography. In: Journal of Chromatography A. 1, Nr. 1, 1958, S. 35–46. doi:10.1016/S0021-9673(00)93398-3.
- J.E. Lovelock: The Electron Capture Detector. In: Journal of Chromatography A. 99, Nr. 1, 1974, S. 3–12. doi:10.1016/S0021-9673(00)90840-9.
- M. Krejči und M. Dressler: Selective Detectors in Gas Chromatography. In: Chromatographic Reviews. 13, Nr. 1, 1970, S. 1–59. doi:10.1016/0009-5907(70)80005-9.
- E.D. Pellizzari: Electron Capture Detection in Gas Chromatography. In: Journal of Chromatography A. 98, Nr. 2, 1974, S. 323–361. doi:10.1016/S0021-9673(00)92077-6.