Betalaine
Betalaine sind eine Gruppe chemisch sehr ähnlicher wasserlöslicher Blüten- und Fruchtfarbstoffe, die neben Anthocyanen und Carotinoiden die dritte Gruppe pflanzlicher Farbstoffe bilden. Sie kommen ausschließlich in nelkenartigen Pflanzen (ausgenommen Nelkengewächse und Molluginaceae) sowie Blätterpilzen vor. Pharmakologisch handelt es sich um ungiftige Alkaloide, die auch antioxidative Eigenschaften aufweisen, wodurch sie medizinisch interessant sind. Etwa 10 bis 14 Prozent der Bevölkerung kann Betalaine nicht vollständig abbauen und scheidet den Farbstoff im Urin aus (sogenannte Beturie, da hauptsächlich nach Genuss von Roter Bete vorkommend). Chemisch handelt es sich um Verbindungen der Betalaminsäure mit verschiedenen Liganden. Je nach Ligand können die Betalaine in die Gruppe der rotvioletten Betacyane sowie die Gruppe der gelben Betaxanthine unterteilt werden.

_1.jpg.webp)
Betalaine können von anderen ähnlichen wasserlöslichen Farbstoffen durch ihre Spektral- und elektrophoretischen Eigenschaften und dadurch unterschieden werden, dass sie in heißem saurem Milieu zerfallen.
In den 1960er-Jahren bestimmten Hugo Wyler und andere die Grundstruktur der Betalaine.[1] Ebenso wurden in dieser Zeit die wichtigsten Reaktionen der Betalain-Biosynthese aufgeklärt. Betalainproduzierende Pflanzen sind nicht in der Lage, Flavan-3,4-diole in Anthocyanidine umzuwandeln, daher kommen Anthocyane und Betalaine nicht gemeinsam vor.
Biosynthese
Im ersten Schritt des Biosyntheseweges wird L-Tyrosin durch 3-Hydroxylierung mittels eines Cytochrom P450-Enzyms zu L-3,4-Dihydroxyphenylalanin (L-Dopa) umgewandelt.[2] Bei Dopa verzweigt sich die Biosynthese: a) einerseits erfolgt seine Oxidation mittels eines CYP-Enzyms zu cyclo-Dopa;[2] b) andererseits wird der aromatische Ring des Dopa durch eine Dopa-4,5-dioxygenase[3] zu seco-Dopa geöffnet, aus dem durch spantane Rezyklisierung Betalaminsäure entsteht. Diese reagiert dann einerseits spontan mit cyclo-Dopa zu Betanidin, oder andererseits nach seiner vorherigen Glucosylierung mittels einer cyclo-Dopa-Glucosyltransferase[4] zu rot-violettem Betanin, dem einfachsten Betacyan. Darüber hinaus reagiert Betalaminsäure spontan mit verschiedenen Aminosäuren oder Aminen zu gelb-orangefarbigen Betaxanthinen (siehe Abbildung). Die Vielfalt der Betacyane entsteht durch unterschiedliche Glucosylierung des Betanidins und seine anschließende Acylierung mit aliphatischen und aromatischen Carbonsäuren.

Betacyane
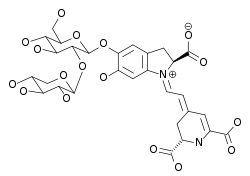
Alle Betacyane weisen einen purpurnen Farbton auf. Der bekannteste Vertreter der Betacyane ist das in der Lebensmittel- und Kosmetikindustrie zugelassene Betanin (Beetenrot). Nachfolgend eine Liste anderer bekannter Betacyane:
- Amaranthin. In Blüten und Blättern vieler Fuchsschwanzgewächse.
- Betanidin. In Blüten von Mesembryanthemum (Mittagsblumengewächse) und Portulaca (Portulakgewächse).
- Bougainvillein-r-1. In Brakteen von Bougainvillea.
- Celosianin II. In Celosia und Gänsefußgewächsen
- Isobetanin. In Früchten von Opuntien und Phyllokladien von Phyllocactus, sowie in Blüten von Mesembryanthemum.
- Muscapurpurin. Bestandteil der roten Farbe des Fruchtkörpers des Fliegenpilzes.
- Prebetanin. In der Haut von Rüben und Früchten der Kermesbeerengewächse.
- Betalaine (Betacyane und Betaxanthine) besitzen auf Grund ihrer antioxidativen Wirkung gesundheitliche Bedeutung.[5]
Betaxanthine
Alle Betaxanthine sind gelb. Hier mehrere bekannte Mitglieder der Gruppe:
- Dopaxanthin. In Blüten von Glottiphyllum (Mittagsblumengewächse).
- Humilixanthin. In Rüben, Mittagsblumengewächsen, Portulakgewächsen und Kermesbeerengewächsen.
- I. Muscaaurin, II und VII. Bestandteil der roten Farbe des Fruchtkörpers des Fliegenpilzes, aber auch in Rüben.
- I. Portulacaxanthin, II und III. In Portulakgewächsen.
- I. Vulgaxanthin und II. In Rüben.
Literatur
- Judith Hans: Klonierung und Charakterisierung von Flavonoidglucosyltransferasen aus Beta vulgaris L. Diss., Martin-Luther-Universität Halle-Wittenberg am 23. Juni 2004. (sundoc.bibliothek.uni-halle.de, Online-Version)
- J. B. Harbourne: Phytochemical Dictionary. Taylor & Francis, 1998, ISBN 0-7484-0620-4, S. 159ff.
- P. Schopfer, A. Brennecke: Pflanzenphysiologie. 6. Auflage. Spektrum Akademischer Verlag, 2006, ISBN 3-8274-1561-6, S. 355 ff.
Einzelnachweise
- H. Wyler: Die Betalaine. In: Chemie in unserer Zeit. Band 3, Nr. 5, 1969, S. 146–151, doi:10.1002/ciuz.19690030504 (PDF (Memento vom 9. Februar 2012 im Internet Archive)).
- G. Polturak u. a.: Elucidation of the first committed step in betalainbosynthesis enables the heterologous engineering of betalain pigments in plants. In: New Phytologist. 2015, doi:10.1111/nph.13796.
- L. Christinet u. a.: Characterization and functional identification of a novel plant 4,5-extradiol dioxygenase involved in betalain pigment biosynthesis in Portulaca grandiflora. In: Plant Physiol. Band 134, 265–274 (2004).
- N. Sasaki u. a.: Detection of UDP-glucose:cyclo-DOPA 5-O-glucosyltransferase activity in four o'clocks (Mirabilis jalapa L.). In: FEBS Lett. Band 568, 2004, S. 159–162 doi:10.1016/j.febslet.2004.04.097.
- E. L. Bastos, W. Schliemann: Betalains as Antioxidants. In: H. M. Ekiert, K. G. Ramawat, J. Arora (Hrsg.): Plant Antioxidants and Health. In: Reference Series in Phytochemistry. Springer, Cham 2021, doi:10.1007/978-3-030-45299-5_9-1.