Acidobacteria
Die Gruppe der Acidobakterien bildet innerhalb der Bakterien ein eigenständiges Phylum. Sie sind also weder mit den Proteobakterien, Firmicutes oder anderen Bakteriengruppen verwandt.
| Acidobacteria | ||||
|---|---|---|---|---|
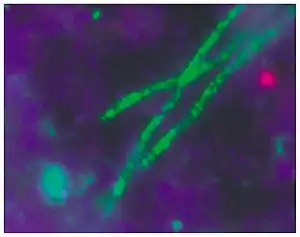
Acidobacterium cf. capsulatum, chemotrophes Bodenbakterium.[1] | ||||
| Systematik | ||||
| ||||
| Wissenschaftlicher Name | ||||
| Acidobacteria | ||||
| Thrash and Coates 2010 |
Der namengebende Organismus für dieses Phylum, Acidobacterium capsulatum, wurde erstmals 1991 aus sauren Bergwerksabwässern in Japan isoliert[2] (lat. acidus: „sauer“) und seine Besonderheit in der phylogenetischen Stellung erkannt[3]. Weitere Bakterienarten, welche ebenfalls zu den Acidobacteria gezählt werden, sind Holophaga foetida[4], Geothrix fermentans[5], Terriglobus roseus[6], Granulicella paludicola, G. pectinivorans, G. aggregans, G. rosea[7], Edaphobacter modestus, E. aggregans[8], Acanthopleuribacter pedis[9] und Chloracidobacterium thermophilum[10]. Neben diesen Organismen lassen sich in der wissenschaftlichen Literatur Hinweise darauf finden, dass noch weitere Isolate vorliegen, welche bisher aber nicht weiter beschrieben sind.
Der bisher geringen Anzahl an isolierten Vertretern der Acidobakterien unter Laborbedingungen steht eine große Anzahl an 16S rDNA-Sequenzen gegenüber. Im Jahr 2007 umfassten die öffentlichen Gendatenbanken über 3000 unterschiedliche Acidobakterium-Sequenzen. Ergebnisse von ersten Untersuchungen zur Phylogenie der Acidobakterien ergaben noch vier bis fünf Untergruppen innerhalb des Phylums[11][12]. Mit wachsender Anzahl an Sequenzen[13][14] aus den unterschiedlichsten Ökosystemen wird seitdem von mindestens 26 Untergruppen ausgegangen[15]. Insgesamt ist das Phylum in seiner phylogenetischen Variabilität vergleichbar mit dem Phylum der Proteobakterien[16].
Vorkommen
Acidobakterien wurden bisher in einer Vielzahl von unterschiedlichen Ökosystemen nachgewiesen. In Böden stellen sie dabei oftmals den Hauptanteil der Bakterien. So lag bei molekularbiologischen Untersuchungen von Böden in Arizona der Anteil von Acidobakterien an der gesamten Bakterienpopulation bei 50 %[17] und in alpinen Böden bei ca. 40 %[18]. Aus Boden-, Wasser- und Sedimentproben isolierte DNA-Fragmente zeigen, dass Acidobakterien weit verbreitet sind. Acidobakterien sind daher wahrscheinlich außerordentlich divers und spielen beim mikrobiell vermittelten Stoffumsatz in der Natur eine wichtige Rolle.
Stoffwechsel
Die große phylogenetische Varianz der Acidobakterien, die vergleichbar mit der der Proteobakterien ist, lässt auf eine ebenso große Variabilität im Stoffwechsel schließen. Bisher liegen zwar nur wenige Acidobakterien in Kultur mit einer größeren Anzahl an Daten zum Metabolismus vor, dennoch scheint sich anhand dieser wenigen Daten die vermutete große Variabilität der Acidobakterien zu bestätigen. Acidobacterium capsulatum wächst langsam und bei geringen Nährstoffkonzentrationen, er bevorzugt oligotrophe Bedingungen. Neuere Untersuchungen weisen darauf hin, dass zumindest einige Acidobakterien auch methylotroph leben können[19].
Systematik
Die folgende Liste folgt LPSN (mit Stand vom 22. Oktober 2020),[20] der Name des Phylums selbst ist nach dieser Quelle noch vorläufig. Es ist nur eine auswahlvon Gattungen und Spezies beispielhaft angegeben:
- Klasse „Acidobacteriia“ Thrash und Coates 2010
- Ordnung Acidobacteriales Cavalier-Smith 2002
- Familie Acidobacteriaceae
- Gattung Acidicapsa Kulichevskaya et al. 2012
- Gattung Acidipila Okamura et al. 2015
- Gattung Acidisarcina Belova et al. 2018
- Gattung Acidobacterium Kishimoto et al. 1991
- Spezies Acidobacterium capsulatum[1]
- Gattung Bryocella Dedysh et al. 2012
- Gattung Chloracidobacterium Tank und Bryant 2015
- Spezies Chloracidobacterium thermophilum
- Gattung Edaphobacter Koch et al. 2008
- Spezies Edaphobacter modestus
- Spezies Edaphobacter aggregans
- Gattung Granulicella Pankratov und Dedysh 2010
- Spezies Granulicella paludicola
- Spezies Granulicella pectinivorans
- Spezies Granulicella aggregans
- Spezies Granulicella rosea
- Gattung Occallatibacter Foesel et al. 2016
- Gattung Silvibacterium Lladó et al. 2016
- Gattung Telmatobacter Pankratov et al. 2012
- Gattung Terracidiphilus García-Fraile et al. 2016
- Gattung Terriglobus Eichorst et al. 2007
- Spezies Terriglobus roseus
- Ordnung Bryobacterales
- Familie Bryobacteraceae
- Spezies Bryobacter aggregatus
- Klasse Blastocatellia
- Ordnung Blastocatellales
- Familie Arenimicrobiaceae
- Familie Blastocatellaceae
- Familie Pyrinomonadaceae
- Klasse Holophagae
- Ordnung Acanthopleuribacterales
- Familie Acanthopleuribacteraceae
- Spezies Acanthopleuribacter pedis
- Ordnung Holophagales
- Familie Holophagaceae
- Spezies Holophaga foetida
- Ordnung Thermotomaculales
- Familie Thermotomaculaceae
- Klasse Thermoanaerobaculia
- Ordnung Thermoanaerobaculales
- Familie Thermoanaerobaculaceae
- Klasse Vicinamibacteria
- Ordnung Vicinamibacterales
- Familie Vicinamibacteraceae
Weblinks
- Just a Few Common Bacterial Groups Gobble Up the Majority of Carbon in Soil, auf: SciTechDaily vom 11. September 2021, Quelle: Lawrence Livermore National Laboratory; sowie Just a Few Common Bacteria Gobble Up Most of the Carbon in Soil, ebenda vom 23. Januar 2022, Quelle: U.S. Department of Energy; über Acidobacteria RB41[21]
Einzelnachweise
- A. L. Baker: PhycoKey: Acidobacteria (Chemo-, Photosynthetic Bacteria), University of New Hampshire
- N. Kishimoto, Y. Kosako, T. Tano: Acidobacterium capsulatum gen. nov., sp. nov.: an acidophilic chemoorganotrophic bacterium containing menaquinone from acidic mineral environment. Curr Microbiol 22: S. 1-7 (1991).
- A. Hiraishi, N. Kishimoto, Y. Kosako, N. Wakao, T. Tano: Phylogenetic position of the menaquinone-containing acidophilic chemo-organotroph Acidobacterium capsulatum. FEMS Microbiol Lett 132, S. 91–94 (1995).
- F. Bak, K. Finster and F. Rotfuß. Formation of dimethylsulfide and methanethiol from methoxylated aromatic compounds and inorganic sulfide by newly isolated anaerobic bacteria. Arch Microbiol 157: S, 529-534 (1992)
- J. D. Coates, D. J. Ellis, C. V. Gaw, D. R. Lovley: Geothrix fermentans gen. nov., sp. nov., a novel Fe(III)-reducing bacterium from a hydrocarbon-contaminated aquifer. International Journal of Systematic and Evolutionary Microbiology, 49: S. 1615–1622, 1999.
- S. A. Eichorst, J. A. Breznak, T. M. Schmidt: Isolation and characterization of soil bacteria that define Terriglobus gen. nov., in the phylum Acidobacteria. Appl Environ Microbiol 73: S. 2708-2717 (2007).
- I. S. Kulichevskaya, N. E. Suzina, W. Liesack, S. N. Dedysh: Bryobacter aggregatus gen. nov., sp. nov., a peat-inhabiting, aerobic chemo-organotroph from subdivision 3 of the Acidobacteria. Int J Syst Evol Microbiol 60: S. 301–306 (2010)
- I. H. Koch, F. Gich, P. F. Dunfield, J. Overmann: Edaphobacter modestus gen. nov., sp. nov., and Edaphobacter aggregans sp. nov., acidobacteria isolated from alpine and forest soils. Int J Syst Evol Microbiol 58: S. 1114–1122 (2008)
- Y. Fukunaga, M. Kurahashi, K. Yanagi, A. Yokota, S. Harayama: Acanthopleuribacter pedis gen. nov., sp. nov., a marine bacterium isolated from a chiton, and description of Acanthopleuribacteraceae fam. nov., Acanthopleuribacterales ord. nov., Holophagaceae fam. nov., Holophagales ord. nov. and Holophagae classis nov. in the phylum ‘Acidobacteria’. Int J Syst Evol Microbiol 58: S. 2597-2601 (2008).
- D. A. Bryant, A. M. G. Costas, J. A. Maresca, A. G. M. Chew, C. G. Klatt, M. M. Bateson, L. J. Tallon, J. Hostetler, W. C. Nelson, J. F. Heidelberg, D. M. Ward: Candidatus Chloracidobacterium thermophilum: An aerobic phototrophic acidobacterium. Science, 317:523–526 (2007).
- C. R. Kuske, S. M. Barns, J. D. Busch: Diverse uncultivated bacterial groups from soils of the arid southwestern United States that are present in many geographic regions. Appl. Environ. Microbiol. 63:3614–3621 (1997).
- W. Ludwig, S. H. Bauer, M. Bauer, I. Held, G. Kirchhof, R. Schulze, I. Huber, S. Spring, A. Hartmann, K. H. Schleifer: Detection and in situ identification of representatives of a widely distributed new bacterial phylum. FEMS Microbiol. Lett. 153:181–190 (1997).
- P. Hugenholtz, B. M. Goebel, N. R. Pace: Impact of cultureindependent studies on the emerging phylogenetic view of bacterial diversity. J. Bacteriol. 180: S. 4765–4774 (1998).
- J. Zimmermann, J. M. Gonzalez, C. Saiz-Jimenez, W. Ludwig: Detection and phylogenetic relationships of highly diverse uncultured acidobacterial communities in Altamira Cave using 23S rRNA sequence analysis. Geomicrobiol. J. 22: S. 379–388 (2005).
- S. M. Barns, E. C. Cain, L. Sommerville, C. R. Kuske: Acidobacteria phylum sequences in uranium-contaminated subsurface sediments greatly expand the known diversity within the phylum. Appl. Environ. Microbiol., 73(9): S. 3113–3116 (2007).
- P. Hugenholtz et al.: Impact of Culture-Independent Studies on the Emerging Phylogenetic View of Bacterial Diversity. In: J. Bact. 180 (18), S. 4765–4774 (1998)
- J. Dunbar, S. M. Barns, L. O. Ticknor, and C. R. Kuske. Empirical and theoretical bacterial diversity in four Arizona soils. Appl. Environ. Microbiol. 68:3035–3045 (2002).
- D. A. Lipson, and S. K. Schmidt. Seasonal changes in an alpine soil bacterial community in the Colorado Rocky Mountains. Appl. Environ. Microbiol. 70:2867–2879 (2004).
- S. Radajewski, P. Ineson, N. R. Parekh and J. Colin Murrell. Stable-isotope probing as a tool in microbial ecology. Nature 403, 646–649 (2000).
- LPSN: Phylum "Acidobacteria"
- NCBI: Acidobacteria bacterium RB41 (species)