Fascin
Fascin ist ein kleines, sehr kompaktes Protein mit einem Gewicht von 55 bis 58 Kilodalton, das Aktinfilamente derart bündelt, dass sie mit 10 nm Abstand, starr und parallel verbunden werden. Seine zwei verschiedenen Aktin-Bindungsstellen liegen auf demselben Polypeptid.[1] Die Aktinbindung wird dabei durch Phosphorylierung reguliert.
| Fascin | ||
|---|---|---|
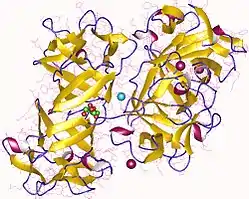 | ||
| Menschliches Fascin | ||
| Andere Namen |
| |
| Eigenschaften des menschlichen Proteins | ||
| Bezeichner | ||
| Gen-Name | FSCN | |
| Externe IDs | ||
Vorkommen und Formen
Ursprünglich isoliert wurde Fascin als eines der ersten Proteine, die Aktin bündeln können, 1982 in Seeigeleiern, man findet es aber auch in Drosophila und in Wirbeltieren.[2][3][4]
Es existieren drei verschiedene Formen von Fascin, die alle von unterschiedlichen Genen codiert werden:[5][6]
- Fascin 1 (FSCN 1), das in Nervenzellen und in unterschiedlichen Mengen anderer Zellen vorkommt
- Fascin 2 (FSCN 2), das in der Netzhaut exprimiert wird, und
- Fascin 3 (FSCN 3), das man nur in den Hoden findet.
Funktion
Fascin ist vor allem in aktinreichen Zellvorsprüngen, den Filopodien lokalisiert und dient dort mit geringer Dissoziation der Stabilisierung von Aktinfilamenten, indem es diese in enge Bündel zusammenpackt. Das erhöht die mechanische Widerstandskraft der Filamente. Das Erstarren des F-Aktin-Netzwerks hat dabei einen plötzlichen Bruch in der Elastizität der Fasern und eine nachfolgende langsame Abnahme zur Folge, ganz im Gegensatz zu alpha-Actinin 3, das die Elastizität erhöht. Die Rate, mit der F-Aktin in Anwesenheit von Fascin erstarrt, ist aber nicht linear abhängig von der Konzentration von Fascin. Untersuchungen haben gezeigt, dass das zum einen daran liegen könnte, dass die Bündelung und Verknüpfung von Aktin mit der weiteren Verzweigung von Aktinfilamenten und -bündeln konkurriert, und zum anderen daran, dass ein verspäteter Zusammenschluss von Aktin mit erhöhter Mikroheterogenität ebenfalls konkurrieren. Weitere Untersuchungen haben Fascin eine Schlüsselrolle bei der Verzweigung von Aktinfilamenten eingeräumt. Die Verzweigung von F-Aktin wiederum fördert die Bildung eines Netzwerks zwischen den Filamenten, was die Beweglichkeit der einzelnen F-Aktinfasern hemmt.[7]
Fascin wird durch Phosphorylierung von Serine 39 durch die Proteinkinase C reguliert.[8]
Klinischer Bezug
Fascin wird in allen menschlichen Geweben in unterschiedlichem Maße exprimiert, aber die Expression scheint in Tumorzellen stark erhöht zu sein und in Zusammenhang mit der Metastasierung, speziell von Karzinomen der Epithelzellen, zu stehen. Eine Erhöhung an Fascin in Krebszellen könnte diesen weitere Motilität und damit Möglichkeiten zur Invasion in weitere Gewebe verschaffen. Wie genau dies funktioniert ist nicht bekannt, aber Studien zeigen, dass Filopodia an der Zellmotilität beteiligt sind, und dass Fascin Aktin in invasiven Zellfortsätzen (Invadopodia) stabilisiert.[9] Dementsprechend lässt sich Fascin als Marker für eine Tumorerkrankung heranziehen und kann zum Erstellen einer Prognose verwendet werden; allerdings ist es nicht für Krebserkrankungen spezifisch. Auch andere Krankheiten wie eine Infektion mit dem Epstein-Barr-Virus haben das Auftreten von Fascin in bestimmten Zellen (hier: B-Lymphozyten) zur Folge.[10]
Einzelnachweise
- Fascin, Lexikon der Biologie, Spektrum Akademischer Verlag, 1999 Heidelberg.
- J. Bryan, R. Edwards, P. Matsudaira, J. Otto und J. Wulfkuhle: Fascin, an echinoid actin-bundling protein, is a homolog of the Drosophila singed gene product. In: Proceedings of the National Academy of Sciences. 90, Nr. 19, Oktober 1993, S. 9115–9119. PMC 47512 (freier Volltext).
- Robert A. Edwards und Joseph Bryan: Fascins, a family of actin bundling proteins. In: Cell Motility and the Cytoskeleton. 32, Nr. 1, Februar 2005, S. 1–9. doi:10.1002/cm.970320102. PMID 8674129.
- http://omim.org/entry/602689
- Shengyu Yang, Fang-Ke Huang, Jianyun Huang, Shuai Chen, Jean Jakoncic, Alejandra Leo-Macias, Ruben Diaz-Avalos, Lin Chen, J. Jillian Zhang und Xin-Yun Huang: Molecular Mechanism of Fascin Function in Filopodial Formation. In: The Journal of Biological Chemistry. 288, Nr. 1, Januar 2014, S. 274–284. doi:10.1074/jbc.M112.427971. PMC 3537022 (freier Volltext).
- N. Kureishy, V. Sapountzi, S. Prag, N. Anilkumar und J. C. Adams: Fascins, and their roles in cell structure and function. In: BioEssays: News and reviews in molecular, cellular and developmental biology. 24, Nr. 4, April 2002, S. 350–361. PMID 11948621.
- Y. Tseng, E. Fedorov, J. M. McCaffery, S. C. Almo und D. Wirtz: Micromechanics and ultrastructure of actin filament networks crosslinked by human fascin: a comparison with alpha-actinin. In: Journal of Molecular Biology. 10, Nr. 2, Juli 2001, S. 351–366. PMID 11428894.
- Ang Li, John C. Dawson, Manuel Forero-Vargas, Heather J. Spence, Xinzi Yu, Ireen König, Kurt Anderson und Laura M. Machesky: The actin bundling protein fascin stabilizes actin in invadopodia and potentiates protrusive invasion. In: Curriculum Biology. 20, Nr. 4, Februar 2010, S. 339–345. doi:10.1016/j.cub.2009.12.035. PMC 3163294 (freier Volltext).
- Caroline F. Mohr, Martina Kalmer, Christine Gross, Melanie C. Mann, Kai R. Sterz, Arnd Kieser, Bernhard Fleckenstein und Andrea K. Kress: The tumor marker Fascin is induced by the Epstein-Barr virus-encoded oncoprotein LMP1 via NF-κB in lymphocytes and contributes to their invasive migration. In: Cell Communication and Signaling. 12, Nr. 46, Juli 2014. doi:10.1186/s12964-014-0046-x. PMID 25105941. PMC 4222691 (freier Volltext).